
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.常温下,c(H+)/c(OH-)=1010的溶液:Fe2+、K+、NO3-、SO42- |
| B.加入Mg能放出H2的溶液:Na+、Al3+、Cl-、SO42- |
| C.加入苯酚显紫色的溶液:NH4+、K+、Cl-、S2- |
| D.由水电离产生的c(H+)=1×10—12的溶液:NH4+、Na+、AlO2-、HCO3- |
科目:高中化学 来源: 题型:单选题
下列书写的离子方程式中,正确的是
| A.高锰酸钾溶液与乙二酸(草酸)反应:2MnO4-+5C2O42-+16H+®2Mn2++10CO2↑+8H2O |
| B.在NH4HSO4溶液中慢慢滴入等物质的量的NaOH溶液:NH4++OH-®NH3·H2O |
| C.VO2+与酸性高锰酸钾溶液反应:5VO2++MnO4-+H2O®5VO2++Mn2++2H+ |
| D.Fe2+离子被空气氧化:4Fe2++O2+2H2O®4Fe3++4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式不正确的是
| A.醋酸溶液中加入少量氢氧化镁固体:Mg(OH)2+2CH3COOH=Mg2++2CH3COO-+2H2O |
| B.H2O2溶液中加入足量酸性KMnO4溶液:2MnO4-+3H2O2+6H+=2Mn2++6H2O+4O2↑ |
| C.Ca(HCO3)2溶液中加入足量澄清石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D.NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO42—恰好沉淀完全:NH4++H++SO42-+Ba2++2OH-=NH3?H2O+BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列化学事实的描述或解释正确的是
| A.Na2SO3溶液中:c(H+)+c(HSO3-)+2c(H2SO3)=c(OH-) |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C.有些化学反应既属于复分解反应又属于氧化还原反应 |
| D.铜片放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列评价及离子方程式书写正确的是
| 选项 | 离子组 | 评价 |
| A | H+、Fe2+、NO3—、Cl— | 不能大量共存于同一溶液中,因为发生了氧化还原反应4Fe2++NO3—+6H+=4Fe3++2NO↑+3H2O |
| B | Na+、CO32—、Cl—、Al3+ | 不能大量共存于同一溶液中,因为发生了互促水解反应2Al3++3CO32—+3H2O=2Al(OH)3↓+3CO2↑ |
| C | Fe3+、K+、SCN—、Br— | 不能大量共存于同一溶液中,因为有红色沉淀生成 Fe3++SCN—=Fe(SCN)3↓ |
| D | HCO3—、OH—、Na+、Ca2+ | 不能大量共存于同一溶液中,因为发生如下反应 HCO3—+OH—=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在pH=0的溶液中能大量共存的离子组是
| A.Fe3+,K+,SO42-,I- | B.Mg2+,NH4+,NO3-,Cl- |
| C.Na+,K+,SO42-,Al(OH)4一 | D.Ba2+,Na+,NO3-,CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是( )
| A.NH3的水溶液可以导电,说明NH3是电解质 |
| B.标准状况下,6.72 L NO2气体与水完全反应转移电子数为1.204×1023 |
| C.向水中通入氯气发生反应的离子方程式为:Cl2+H2O=2H++Cl-+ClO- |
| D.加入铝片能放出H2的溶液中可能大量共存的离子:Na+、NO3-、NH4+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.无色溶液:K+、Na+、Cu2+、SO42— |
| B.c(OH-)=10-13mol· L-1的溶液:Al3+、NO3—、I-、Cl- |
| C.水电离产生的c(H+)=10-13mol·L-1的溶液:Na+、Cl-、NO3—、SO42— |
| D.0.1 mol·L-1 FeSO4溶液:K+、NH4+、MnO4—、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关说法正确的是( )
| A.1 mol Cl2参加反应转移电子数一定为2NA |
B.在反应KIO3+6HI KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA |
C.根据反应中HNO3(稀)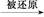 NO,而HNO3(浓) NO,而HNO3(浓)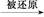 NO2可知,氧化性HNO3(稀)>HNO3(浓) NO2可知,氧化性HNO3(稀)>HNO3(浓) |
| D.含有大量NO3—的溶液中,不能同时大量存在H+、Fe2+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com