
| A. | 该反应是熵减小的反应 | |
| B. | 该反应是吸热反应,因此不能自发进行 | |
| C. | 判断反应能否自发进行需要根据△H与△S综合考虑 | |
| D. | (NH4)2CO3(s)比NH4HCO3(s)稳定 |
分析 A.依据反应的特征分析(NH4)2CO3((s)=NH4HCO3(s)+NH3(g)△H=+74.9kJ•mol-1,反应是熵变增大的反应;
B.反应自发进行的判断依据是△H-T△S<0,反应自发进行;
C.反应能自发,应满足△G=△H-T•△S<0,结合反应的△H和△S进行判断;
D.(NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9kJ/mol,可知1mol的NH4HCO3(s)大于1mol(NH4)2CO3(s),能量越低越稳定.
解答 解:A.依据反应的特征分析(NH4)2CO3((s)=NH4HCO3(s)+NH3(g)△H=+74.9kJ•mol-1,反应是熵变增大的反应,△S>0,故A错误;
B.该反应是吸热反应,△H>0,△S>0;反应自发进行的判断依据是△H-T△S<0,当高温下反应可以自发进行,故B错误;
C.根据△G=△H-T•△S判断反应能否自发进行,△H>0,△S>0,在较高温度下可满足△H-T•△S<0,即在较高温度下反应能自发进行;△H<0,△S<0,温度较低时即可满足△H-T•△S<0,能自发进行;△H>0,△S<0,一般情况下△G=△H-T•△S>0,不能自发进行;△H<0,△S>0,可满足△H-T•△S<0,反应能自发进行,故C正确;
D.(NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9kJ/mol,可知1mol的NH4HCO3(s)大于1mol(NH4)2CO3(s),能量越低越稳定,因此
NH4HCO3(s)比(NH4)2CO3(s)稳定,故D错误;
故选C.
点评 本题考查了反应自发进行的判断依据,理解自发进行的因素是由焓变和熵变温度共同决定,题目较简单.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 56(m-n)g | B. | 56(n-m)g | C. | 56ng | D. | 56(m-2n)g |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
在恒温恒压下,向密闭容器中充入4mol A和2 mol B,发生如下反应:2A(g)+B(g)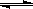 2C(g) ΔH<0。2min后,反应达到平衡,生成C为1.6mol。则下列分析正确的是
2C(g) ΔH<0。2min后,反应达到平衡,生成C为1.6mol。则下列分析正确的是
A.若反应开始时容器体积为2L,则Vc=0.4mol•L-1•min-1
B.若在恒压绝热条件下反应,平衡后nc<1.6mol
C.若2min后,向容器中再投入等物质的量A、C,B的转化率不变
D.若该反应在恒温恒容下进行,放出热量将增加
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保持其它条件不变,加入少量W,平衡将逆向移动 | |
| B. | 保持温度和体积不变,加入少量X,正、逆反应速率均增大 | |
| C. | 保持体积不变,升高温度,正反应速率增大,逆反应速率降低 | |
| D. | 保持温度不变,将体积压缩一半,新平衡时体系压强变为原来的两倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO | B. | N2O | C. | N2 | D. | NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A与B一定都是气体 | B. | 平衡向正反应方向移动了 | ||
| C. | 物质B的质量分数增加了 | D. | a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
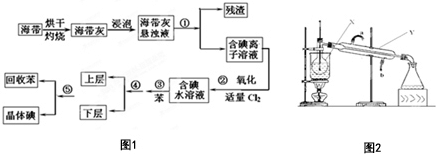 海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室从海带中提取碘的流程图如图1:(已知:Cl2+2I-═2Cl-+I2)
海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室从海带中提取碘的流程图如图1:(已知:Cl2+2I-═2Cl-+I2) 查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取CuO2的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取CuO2的三种方法:| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com