
下表是元素周期表的一部分,回答下列有关问题:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)在①~⑫元素中,金属性最强的元素是________,非金属性最强的元素是________,最不活泼的元素是________。(均填元素符号)
(2)元素⑦与元素⑧相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(3)第3周期中原子半径最大的元素是________(填元素符号),跟它同周期的原子半径最小的元素是________(填元素符号),它们可以形成的化合物的化学式为________。
解析:由题目给出的各元素在元素周期表中的位置,可以判断①~⑫元素分别为N、F、Na、Mg、Al、Si、S、Cl、Ar、K、Ca、Br。
(1)在元素周期表中同一周期从左到右元素的金属性逐渐减弱,非金属性逐渐增强;同一主族从上到下元素的金属性逐渐增强,非金属性逐渐减弱。因此在①~⑫元素中最活泼的金属元素为⑩号元素K,最活泼的非金属元素为②号元素F,最不活泼的元素为⑨号元素Ar。
(2)元素⑦为S,元素⑧为Cl,其非金属性强弱为Cl>S,可以通过其气态氢化物的稳定性或最高价含氧酸的酸性强弱来判断。
(3)第3周期元素原子半径从左到右依次减小(除稀有气体元素外),因此原子半径最大的为Na,最小的为Cl,它们可形成NaCl。
答案:(1)K F Ar (2)Cl b (3)Na Cl NaCl


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
下列对氧化还原反应的分析中不合理的是( )
A.Mg变为MgO时化合价升高,故Mg在该反应中作还原剂
B.在反应2H2S+SO2====3S+2H2O中,氧化产物和还原产物都是S
C.凡是氧化还原反应都有利于生产、生活
D.在反应2H2O 2H2↑+O2↑中,H2O既是还原剂又是氧化剂
2H2↑+O2↑中,H2O既是还原剂又是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合溶液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )
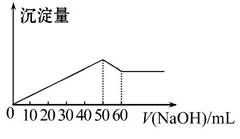
A.6∶1 B.3∶1 C.2∶1 D.1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
某主族元素原子的O层上只有1个电子,下列描述正确的是( )
A.其单质在常温下跟水反应不如钠剧烈
B.其原子半径比钾原子半径小
C.其碳酸盐易溶于水
D.其氢氧化物不能使氢氧化铝溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于铜电极的叙述正确的是( )
A.铜锌原电池中铜是负极
B.用电解法精炼粗铜时粗铜作阴极
C.在镀件上电镀铜时可用铜作阳极
D.电解食盐水时铜作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
检验溶液中是否含有某种离子,下列操作方法正确的是 ( )
A.加入AgNO3溶液,有白色沉淀生成,证明有Cl-
B.用硝酸酸化后取上层清液,加入Ba(OH)2溶液,析出白色沉淀,证明有SO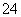
C.加浓NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝色的气体,证明有NH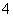
D.加入盐酸,放出能使澄清石灰水变浑浊的气体,证明含有CO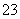
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com