


科目:高中化学 来源: 题型:
| A、常温下由水电离产生的c(H+)=10-12 mol?L-1的溶液中加入铝粉都能够产生氢气 |
| B、已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12.在含Cl-、CrO42-浓度相同的溶液中滴加几滴稀AgNO3溶液时,则先生成AgCl沉淀 |
| C、电解硫酸铜溶液一段时间后,加入氧化铜固体不可能使溶液恢复到原来的浓度 |
| D、实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
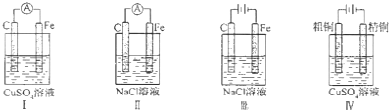
| A、实验Ⅰ:电流表A指针偏转,碳棒上有气泡冒出 |
| B、实验Ⅱ:电流表A指针偏转,铁极上有无色气体产生 |
| C、实验Ⅲ:碳棒上有无色气体产生,铁极上有黄绿色气体产生 |
| D、实验IV:粗铜溶解,精铜上有红色固体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a=b | ||
| B、混合溶液的PH=7 | ||
| C、混合溶液中,PH=14-pOH的溶液 | ||
D、混合溶液中,c(H+)=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、烧碱、冰醋酸、四氯化碳均为电解质 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、福尔马林、水玻璃、氨水均为混合物 |
| D、SO2、SiO2、CO均为酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电镀池的阳极材料必须是镀层金属 |
| B、测量中和反应的反应热时,反应过程中需要记录最高温度 |
| C、原电池工作时,电解质溶液中的阳离子移向负极 |
| D、胶体的本质特征是丁达尔现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com