
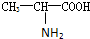 ),苯丙氨酸(
),苯丙氨酸(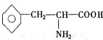 )
)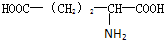 ),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )
),则该多肽中所含肽键的数目以及水解后得到的谷氨酸和苯丙氨酸的数目分别是( )| A. | 10,4,3 | B. | 10,3,4 | C. | 9,4,3 | D. | 9,3,4 |
分析 根据氨基酸在形成多肽时原子数目的变化规律,利用解方程组法解决.
解答 解:观察形成该“多肽”的四种氨基酸的结构特点,每个氨基酸的结构中只有一个氨基,即只含有一个氮原子,在形成肽时,氮原子都进入肽中,这个“多肽”为10肽,含有9个肽键,
根据氨基酸在形成多肽时原子数目的变化规律,利用解方程组法解决;设该10肽中含有甘氨酸、丙氨酸、苯丙氨酸、谷氨酸的个数分别为a、b、c、d,根据题意列方程组得
2a+3b+9c+5d=55
5a+7b+11c+9d-9×2=70
2a+2b+2c+4d-9=19
a+b+c+d=10
解得a=1,b=2,c=3,d=4
所以该10肽水解后有4个谷氨酸,3个苯丙氨酸.
故选A.
点评 本题考查氨基酸、蛋白质的结构和性质特点,把握氨基酸在形成多肽时原子数目的变化规律,是解题的关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 40 | B. | 18 | C. | 12 | D. | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
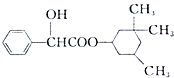 环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物持的叙述中,正确的是( )
环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物持的叙述中,正确的是( )| A. | 该物质属于芳香烃 | |
| B. | 该有机物难溶于水 | |
| C. | 分子式为C17H23 | |
| D. | 1mol该物质最多可与2molNaOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X中阳离子和阴离子个数一定相等 | |
| B. | X中可能既含离子键,又含共价键 | |
| C. | 若X只含两种元素,则两种元素可在同一周期也可在同一主族 | |
| D. | X中阳离子半径一定大于阴离子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
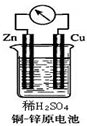 如图所示的铜-锌原电池中,理论上应观察到的现象是:
如图所示的铜-锌原电池中,理论上应观察到的现象是:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com