
| 选项 | 实验事实 | 理论解释 |
| A | N原子的第一电离能大于O原子 | N原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C=O之间的夹角为120° |
| C | 金刚石的熔点低于石墨 | 金刚石是原子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A. | A | B. | B | C. | C | D. | D |
分析 A.原子轨道处于半满、全满或全空时原子最稳定;
B.二元化碳分子为直线形分子,键角为180°;
C.石墨不是原子晶体,金刚石的原子晶体大于石墨;
D.氟化氢的相对分子质量小于氯化氢,氢键的存在导致HF的沸点较高.
解答 解:A.原子轨道处于半满、全满或全空时原子最稳定,N原子2p轨道电子半充满,所以N原子不容易失去电子,所以N原子的第一电离能大于O原子,故A正确;
B.二氧化碳的价层电子对个数是2,所以二元化碳分子为直线形分子,则二氧化碳分子的键角为180°,故B 挣钱;
C.金刚石为原子晶体,石墨为混合型晶体,所以金刚石熔点高于石墨,故C错误;
D.卤族元素氢化物都属于分子晶体,分子晶体的沸点与其相对分子质量成正比,但氟化氢中含有氢键,氯化氢中不含氢键,导致氟化氢沸点高于HCl,故D错误-故选C.
点评 本题考查较综合,涉及氢键、键角、第一电离能、晶体类型与熔点的关系等知识点,知道氢键对物质沸点的影响、晶体类型与晶体熔点的关系等知识点即可解答,注意氢键属于分子间作用力而不是化学键,为易错点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 还原性:S2-<Cl-<F- | B. | 稳定性:HF>HCl>H2S | ||
| C. | 碱性:KOH<NaOH<Al(OH)3 | D. | 还原性:K>Na>Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
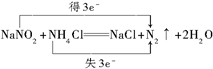 (并标出电子转移的数目和方向).
(并标出电子转移的数目和方向).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将一定体积醋酸溶液加水到原来体积的m倍,则pH增大m | |
| B. | 在NaHCO3溶液中,c(Na+)=c(HCO3-)+c(H2CO3) | |
| C. | 25℃,pH=8的NaOH溶液和pH=8的氨水中,由水电离出的c(OH-)不相等 | |
| D. | 25℃,pH=13的Ba(OH)2溶液和pH=1的盐酸中均存在:c(H+)•c(OH-)=1×10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H2含碳量最高,燃烧生成的CO2最多 | |
| B. | C2H4燃烧生成水与CO2的物质的量相等 | |
| C. | CH4含氢量最高,燃烧生成水最多 | |
| D. | CH4、C2H4燃烧生成水的质量不相同,消耗氧气不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=3的某酸溶液与pH=11的NaOH溶液等体积混合后,溶液pH≤7 | |
| B. | 将某电解质溶液加水稀释,溶液中离子浓度都减小 | |
| C. | 酸所能提供的H+与碱所能提供的OH-的物质的量相等即酸碱完全中和 | |
| D. | 在某盐溶液中,可能存在大量的Na+、Ba2+、AlO2-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,3-二甲基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 3-甲基-3-乙基戊烷 | D. | 2,2,3,3-四甲基丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和② | B. | ①和③ | C. | ③和④ | D. | ②和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石的能量比石墨高,因此金刚石比石墨更稳定 | |
| B. | 化学反应中的能量变化主要是由化学键变化引起的 | |
| C. | 浓硫酸溶于水会放出大量热,这属于放热反应 | |
| D. | 木炭需加热到一定温度时才燃烧,所以木炭燃烧是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com