
【题目】“雾霾”成为人们越来越关心的环境问题.雾霾中含有二氧化硫、氮氧化物和可吸入颗粒物等污染性物质.请回答下列问题:
(1)汽车尾气是雾霾形成的原因之一.尾气治理可用汽油中挥发出来的烃类物质 (CxHy)催化还原尾气中的NO气体,该过程的化学方程式为 .
(2)冬季燃煤供暖产生的废气也是雾霾的主要来源之一.经研究发现将煤炭在 ![]() 的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为: . 2NO(g)+2CO(g)N2(g)+2CO2 (g)△H
的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为: . 2NO(g)+2CO(g)N2(g)+2CO2 (g)△H
已知:
①N2(g)+O2(g)2NO(g)△H1=+180.5kJmol﹣1
②2CO(g)2C(s)+O2(g)△H2=+221kJmol﹣1
③C(s)+O2(g)CO2(g)△H3=﹣393.5kJmol﹣1
则△H=
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图一所示,电极材料为石墨. 
①a表示离子交换膜(填“阴”或“阳”).A﹣E分别代表生产中的原料或产品.其中C为硫酸,则A表示 . E表示 .
②阳极的电极反应式为 .
(4)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的 反应为:2SO2(g)+O2(g)2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2):n(O2)=2:1],测得容器内总压强与反应时间如图二所示.
①图中A点时,SO2的转化率为 .
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,刻C点的正反应
速率vc(正)与A点的逆反应速率vc (逆)的大小关系为vc(正)vc (逆) (填“>”、“<”或“=”)
③图中B点的压强平衡常数kp=(用平衡分压代替平衡浓度计算.分压=总压×物质的量分数).
【答案】
(1)4CxHy+(8x+2y)NO=4XCO2+(4x+y)N2+2yH2O
(2)2NO(g)+2CO(g)?N2(g)+2CO2(g);﹣746.5kJ?mol﹣1
(3)阳;NaOH溶液;氢气;SO32﹣﹣2e﹣+H2O=2H++SO42﹣
(4)45%;>
【解析】解:(1)(CxHy)催化还原尾气中的NO气体生成氮气、二氧化碳和水,结合原子守恒配平书写化学方程式为:4CxHy+(8x+2y)NO=4XCO2+(4x+y)N2+2yH2O,所以答案是:4CxHy+(8x+2y)NO=4XCO2+(4x+y)N2+2yH2O;(2)②×2+③×2﹣①得到2NO(g)+2CO(g)N2(g)+2CO2(g),反应的焓变=2(+110.5kJmol﹣1)+2(﹣393.5kJmol﹣1)﹣(180.5kJmol﹣1)=﹣746.5kJmol﹣1 ,
所以答案是:﹣746.5kJmol﹣1;(3)①从C为硫酸可知,硫酸根来源于亚硫酸根放电.故b为阴离子交换膜,a为阳离子交换膜,在阴极区应为水放电生成氢气和氢氧根离子,故A为氢氧化钠,E为氢气,
所以答案是:阳;NaOH溶液;氢气;②阳极应为亚硫酸根放电生成硫酸根,反应的离子方程式为SO32﹣﹣2e﹣+H2O=2H++SO42﹣ ,
所以答案是:SO32﹣﹣2e﹣+H2O=2H++SO42﹣;(4)①依据化学三行列式计算,设氧气消耗物质的量为x,
2SO2(g)+ | O2(g) | 2SO3 | |
起始量(mol) | 2a | a | 0 |
变化量(mol) | 2x | x | 2x |
平衡量(mol) | 2a-2x | a-x | 2x |
图中A点时,气体物质的量0.085,则 ![]() =
= ![]() ,x=0.45a
,x=0.45a
SO2的转化率= ![]() ×100%=45%,
×100%=45%,
所以答案是:45%;②图象分析可知,先拐先平温度高则T1<T2 , C点是平衡状态,A点反应未达到平衡状态,其中C点的正反应速率vC(正)与A点的逆反应速率vA(逆)的大小关系为vC(正)>vA(逆)
所以答案是:>;③图中B点,依据化学三行列式计算,设氧气消耗物质的量为y,
2SO2(g)+ | O2(g) | 2SO3 | |
起始量(mol) | 2a | a | 0 |
变化量(mol) | 2y | y | 2y |
平衡量(mol) | 2a-2y | a-y | 2y |
B点气体物质的量为 0.007,则 ![]() =
= ![]() ,y=0.9a,
,y=0.9a,
平衡常数K=(  =24300(MPa)﹣1 ,
=24300(MPa)﹣1 ,
所以答案是:24300(MPa)﹣1 .
【考点精析】本题主要考查了反应热和焓变和化学平衡的计算的相关知识点,需要掌握在化学反应中放出或吸收的热量,通常叫反应热;反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】X,Y,Z,W均为短周期元素,它们在元素周期表中的位置如下图所示.若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( ) ![]()
A.氢化物稳定性:X>Y
B.最高价氧化物对应的水化物的酸性:W>Y
C.4种元素的单质中,W单质的熔、沸点最高
D.干燥的W单质具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( ) 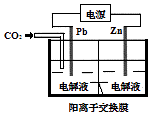
A.Pb与电源的正极相连
B.ZnC2O4在离子交换膜右侧生成
C.正极反应式为:Zn﹣2e﹣═Zn2+
D.标准状况下,当11.2 L CO2参与反应时,转移0.5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,某化合物X受热分解:2X=A↑+2B↑+4C↑。测得反应后生成的混合气体对H2的相对密度为d,在相同条件下,X的相对分子质量是
A. 2d B. 7d C. 5d D. 3.5d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,△H能正确表示物质的燃烧热的是( )
A.CO(g)+ ![]() O2(g)═CO2(g);△H=﹣283.0 kJ/mol
O2(g)═CO2(g);△H=﹣283.0 kJ/mol
B.C(s)+ ![]() O2(g)═CO(g);△H=﹣110.5 kJ/mol
O2(g)═CO(g);△H=﹣110.5 kJ/mol
C.H2(g)+ ![]() O2(g)═H2O(g);△H=﹣241.8 kJ/mol
O2(g)═H2O(g);△H=﹣241.8 kJ/mol
D.2C8H18(l)+25O2(g)═16CO2(g)+18H2O(l);△H=﹣11036 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼是一种重要的化工原料,某同学设计的三氯化硼制备装置如图. 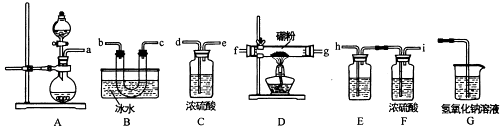
【查阅资料】
①BCl3:的熔点为﹣107.3℃,沸点为12.5℃
②2B+6HCl ![]() 2BCl3+3h2
2BCl3+3h2
③硼与侣的性质相似,也能与氢氧化钠溶液反应
请回答下列题:
(1)A装置可用高高锰酸钾固体与浓盐酸反应制氯气,反应的化学方程式为 .
(2)为了完成三氯化硼的制备,装置从左到右的接口连接顺序为 .
(3)装里E中的试剂为 . 如果拆去E装置,可能的后果是 .
(4)D装置中发生反应前先通入一段时间的氯气,其目的是 . 该装置中发生反应的化学方程式为 .
(5)三氯化硼与水能剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式 .
(6)请设计一个简易实验,验证制得的产品中是否含有硼粉 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=;若其他条件不变,容器体积缩小为1L,则K值 . (增大、减小或不变);若K300°C>K350°C , 则该反应是热反应.
(2)用O2表示从0~2s内该反应的平均速率v=;
(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效催化剂.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解。请你和他一起通过下图所示Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。
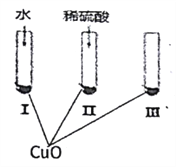
(1)通过实验I可以证明___________________。
(2)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步确认的实验操作是:在Ⅲ中先加入__________,再加入_________。
(3)探究结果为__________ 。
(4)反应的离子方程式为__________。
【答案】 水不能使氧化铜溶解 可溶性硫酸盐 稀硫酸 H+能溶解氧化铜,而H2O、SO42-两种离子都不能使CuO溶解 CuO+2H+=Cu2++H2O
【解析】(1)实验Ⅰ的试管中的液体成分为水,该实验证明水不溶解CuO;
(2)要想证明起作用的是H+,首先要排除SO42-的干扰,所以在Ⅲ中应该加入可溶性硫酸盐,如Na2SO4(或K2SO4等),最后再加放稀硫酸;
(3)通过对比实验验证起作用的成分,得出结论是:氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解;
(4)CuO与硫酸电离的氢离子反应生成铜离子和水,反应的离子方程式为:CuO+2H+=Cu2++H2O。
点睛:性质实验方案设计的一般思路、程序是: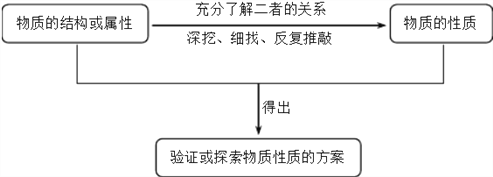 。
。
【题型】实验题
【结束】
28
【题目】(1)己知: 将Cl2通入适量KOH 溶液,产物中可能有KC1、KClO、KC1O3,且c(Cl-):c(C1O-)的值与温度高低有关。当n(KOH)=amol时,若某温度下,反应后c(Cl-):c(C1O-)=11,则溶液中c(ClO-):c(ClO3-)=__________。
(2)在P+CuSO4+H2O→CuP+H3PO4+H2SO4(未配平)的反应中,7.5molCuSO4 可氧化P的物质的量为_______mol。生成1molCu3P时,参加反应的P 的物质的量为_______mol。
(3)一定量的CuS和Cu2S 的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-) 加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO16.0g,若上述气体为NO和NO2的混合物,且体积比为1:1,则V的极小值为______L。
(4)向一定量的Fe、FeO、Fe3O4的混合物中,加入1mol/L 硝酸的溶液100mL,恰好使混合物全部溶解,且放出336mLNO (标准状况下),向所得溶液中加入KSCN 溶液,溶液无红色出现; 若取相同质量的Fe、FeO、Fe3O4的混合物,加入1mol/L 的稀硫酸溶液,也恰好使混合物完全溶解(假设还原产物唯一),反应后向所得溶液中加入KSCN溶液,溶液也无红色出现,则所加入的的稀硫酸的体积是______mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】福莫特罗是一种治疗哮喘病的药物,它的关键中间体(G)的合成路线如下: 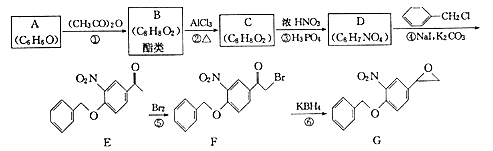
回答下列问题:
(1)F中的含氧官能团有(填名称);反应④的反应类型为 .
(2)反应①的化学方程式为 .
(3)C能与FeCl3溶液发生显色反应,C的结构简式为;D的结构简式为 .
(4)B的同分异构体(不含立体异构)中能同时满足下列条件的共有种. a.能发生银镜反应 b.能与NaOH溶液发生反应 c.含有苯环结构
其中核磁共振氢谱显示为4组峰,且峰面积比为3:2:2:1的是(填结构简式)
(5)参照G的合成路线,设计一种以 ![]() 为起始原料制备
为起始原料制备 ![]() 的合成路线:
的合成路线:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com