
如图是Fe和Cu形成的原电池,某实验兴趣小组做完实验 后,在读书卡片上记录如下,其中正确的是
后,在读书卡片上记录如下,其中正确的是
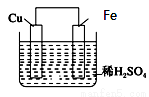
①Fe为正极,Cu为负极;
②H+向负极移动;
③电子是由Fe经外电路流向Cu;
④Cu极上有H2产生;
⑤若有1 mol电子流过导线,则产生的H2为11.2L;
⑥负极的电极反应式为Fe-3e-===Fe3+
A.①②③ B.③④ C.③④⑤ D.③④⑥
 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源:2015-2016学年福建省高一下期末化学试卷(解析版) 题型:选择题
对于反应A(g)+3B(g) 2C(g)+2D(g)来说,下列四种不同情况下的反应速率最快的是
2C(g)+2D(g)来说,下列四种不同情况下的反应速率最快的是
A.v (A)=0.15 mol/(L?s)
B.v(B)=0.6 mol/(L?s)
C.v(C)=0.4 mol/(L?s)
D.v(D)=0.45 mol/(L?s)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一创新班下期末化学试卷(解析版) 题型:选择题
近年来,我国在超导材料研究方面居于世界领先地位,铊(Tl)是超导体的组成成分之一,铊位于第六周期第IIIA族。下列对铊的可能性质的推导正确的是( )
①原子半径比Al大 ②Tl(OH)3是两性氢氧化物
③Tl3+氧化能力比Al3+强 ④单质能与稀硝酸反应生成硝酸盐
A. ①④ B. ②③ C. 只有① D. 只有④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都外国语学校高一下期末理科化学卷(解析版) 题型:选择题
具有如下电子层结构的原子,其相应元素一定属于同一主族的是
A. 2p能级上只有1个空轨道的原子和3p能级上只有1个空轨道的原子
B. 最外层电子排布为3s2的原子和最外层电子排布为4s2的原子
C. 最外层电子排布为ns2的原子和最外层电子排布为ns2np6的原子
D. 2p能级上有2个未成对电子的原子和3p能级上有2个未成对电子的原子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都外国语学校高一下期末理科化学卷(解析版) 题型:选择题
图甲和图乙表示的是短周期部分或全部元素的某种性质的递变规律,下列说法正确的是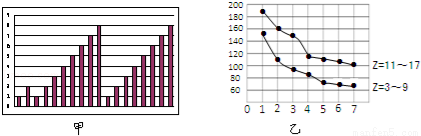
A. 图甲横坐标为原子序数,纵坐标表示元素的最高正价
B. 图甲横坐标为核电荷数,纵坐标表示元素的原子半径(单位:pm)
C. 图乙横坐标为最高正价,纵坐标表示元素的原子半径(单位:pm)
D. 图乙横坐标为最外层电子数,纵坐标表示元素的原子半径(单位:pm)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都外国语学校高一下期末理科化学卷(解析版) 题型:选择题
下列关于化学用语的表述正确的是
A.原子核内有8个中子的碳原子
B.基态氧原子核外电子的轨道表示式: 
C.HClO的结构式为H-Cl-O
D.Ca2+的结构示意图为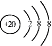 ,NH4Cl的电子式为
,NH4Cl的电子式为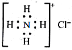
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
在恒容密闭容器中通入X并发生反应:2X(g)  Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是

A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,v(Y)= mol·L-1·min-1
mol·L-1·min-1
C.M点的正反应速率v正大于N点的逆反应速率v逆
D.M点时再加入一定量X,平衡后X的转化率减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:简答题
【加试题】烟气的主要污染物是SO2、NOx,经臭氧预处理后再用适当溶液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9 kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2 kJ·mol-1
SO2(g)+O3(g) SO3(g)+O2(g) △H=-241.6 kJ·mol-1
SO3(g)+O2(g) △H=-241.6 kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的 △H=_ ______ kJ·mol-1。
(2)臭氧脱硝反应2NO2(g)+O3(g) N2O5(g)+O2(g)能自发进行。在温度为T1K时,向体积为2L的恒容密闭容器中充入1 mol O3和2 mol NO2,发生上述反应,经25分钟反应达平衡,测得平衡时N2O5(g)的浓度为0.25 mol·L-1。
N2O5(g)+O2(g)能自发进行。在温度为T1K时,向体积为2L的恒容密闭容器中充入1 mol O3和2 mol NO2,发生上述反应,经25分钟反应达平衡,测得平衡时N2O5(g)的浓度为0.25 mol·L-1。
①判断该反应的△S__ _____0,△H_ ______0(填>、<或=)。
②在温度为T1K时该反应的平衡常数K= 。
③下列说法正确的是 。
A.从反应开始到达平衡,NO2的平均反应速率v(NO2)=0.04mol·L-1·min-1
B.T1K时,若起始时向容器中充入1 mol O3、2 mol NO2、1 mol O2和1 mol N2O5气体,则反应达到平衡前v(正) <v(逆)
C.若改变反应温度为T2K,测得平衡时NO2的浓度为0.60 mol·L-1,则T2>T1
D.T1K时反应达平衡时容器的体积为2L,若维持T1K压缩容器使NO2转化率为60%,则此时容器的体积约为0.71L
④若维持其他条件不变,仅改变温度为T2K时,经15分钟反应达平衡,测得平衡时N2O5(g)的浓度为0.20 mol·L-1。画出在T2K下从0到25分钟c(NO2)随时间变化图。
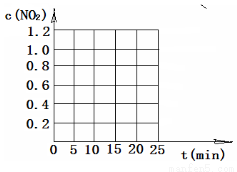
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:选择题
25℃时,甲、乙两烧杯均盛有5mLpH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4。下列关于甲烧杯和稀释后的乙烧杯中的溶液的描述中,不正确的是
A.溶液的体积:10V甲≤V乙
B.水电离出的OH-浓度:10c(OH-)甲=c(OH-)乙
C.若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙
D.若分别与5mLpH=11的NaOH溶液反应,所得溶液的pH:甲≤乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com