
¹¤ŅµÉĻŅ²æÉŅŌÓĆCO2ŗĶH2·“Ó¦ÖĘµĆ¼×“¼”£ŌŚ2”Į105Pa”¢300”ęµÄĢõ¼žĻĀ£¬ČōÓŠ44g CO2Óė6g H2Ē”ŗĆĶźČ«·“Ӧɜ³ÉĘųĢå¼×“¼ŗĶĖ®£¬·Å³ö49.5kJµÄČČĮ攣ŹŌŠ“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
ij“ĪŹµŃ齫6molCO2ŗĶ8molH2³äČė2LµÄĆܱÕČŻĘ÷ÖŠ£¬²āµĆH2µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆČēĻĀĶ¼ĖłŹ¾£ØŹµĻߣ©”£
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ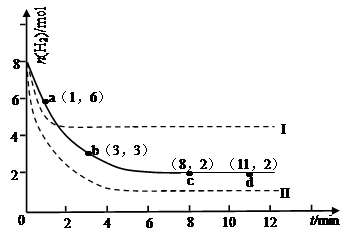
£Ø1£©aµćÕż·“Ó¦ĖŁĀŹ £ØĢī“óÓŚ”¢µČÓŚ»ņŠ”ÓŚ£©Äę·“Ó¦ĖŁĀŹ”£
£Ø2£©ĻĀĮŠŹ±¼ä¶ĪĘ½¾ł·“Ó¦ĖŁĀŹ×ī“óµÄŹĒ £¬×īŠ”µÄŹĒ ”£
| A£®0”«1min |
| B£®1”«3min |
| C£®3”«8min |
| D£®8”«11min |
CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ”÷H= £49.5kJ”¤mol-1
£Ø3·Ö£¬·½³ĢŹ½2·Ö£¬”÷HµÄ±ķŹ¾1·Ö£¬»ÆѧŹ½”¢×“Ģ¬“ķĪó0·Ö£»£”¢ģŹ±äŹżÖµ”¢µ„Ī»“ķĀ©ŗĻæŪ1·Ö£»¼ĘĮæŹżÓĆ·ÖŹż±ķŹ¾ÓėģŹ±äĻąĘ„ÅäŅ²øų·Ö£©
£Ø1£©“óÓŚ £Ø2·Ö£© £Ø2£©A£Ø1·Ö£©£¬ D £Ø1·Ö£©
£Ø3£©
CO2£Øg£©£«3H2£Øg£© CH3OH£Øg£©£«H2O£Øg£©
CH3OH£Øg£©£«H2O£Øg£©
ĘšŹ¼ĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 3 4 0 0
×Ŗ»ÆĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 1 3 1 1
Ę½ŗāĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 2 1 1 1 £Ø1·Ö£©
H2µÄ×Ŗ»ÆĀŹ=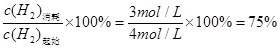 »ņ0.75
»ņ0.75
£Ø2·Ö£¬ÓĆ·ÖŹż±ķŹ¾æŪ1·Ö,“śČėŹżÖµ²»“ųµ„Ī»²»æŪ·Ö£¬²»æ¼ĀĒÓŠŠ§Źż×Ö£©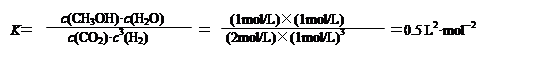 £Ø3·Ö£©
£Ø3·Ö£©
£ØĘäÖŠĮŠŹ½1·Ö£¬“śČėŹżÖµ1·Ö£¬½į¹ū1·Ö£»½į¹ū”¢µ„Ī»“ķĪóŗĻæŪ1·Ö£¬“śČėŹżÖµ²»“ųµ„Ī»²»æŪ·Ö£¬KÖµ²»“ųµ„Ī»²»æŪ·Ö£¬²»æ¼ĀĒÓŠŠ§Źż×Ö£©
£Ø4£©ÉżøßĪĀ¶Č£Ø2·Ö£© Ōö“óŃ¹Ēæ£Ø2·Ö£©
½āĪöŹŌĢā·ÖĪö£ŗŅŃÖŖ4.4g CO2ĘųĢåÓėH2¾“߻ƼÓĒāÉś³ÉCH3OHĘųĢåŗĶĖ®ÕōĘųŹ±·Å³ö4.95kJµÄÄÜĮ棬Ōņ1mol¶žŃõ»ÆĢ¼Č«²æ·“Ó¦·ÅČČ49.5KJ£»½įŗĻČČ»Æѧ·½³ĢŹ½ŹéŠ“·½·ØŠ“³öČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO2£Øg£©+3H2£Øg£©=CH3OH£Øg£©+H2O£Øg£©”÷H=-49.5KJ/mol£»
¹Ź“š°øĪŖ£ŗCO2£Øg£©+3H2£Øg£©=CH3OH£Øg£©+H2O£Øg£©”÷H=-49.5KJ/mol£»
£Ø1£©øł¾ŻĶ¼ĻóæÉÖŖ£¬aµ½b¹ż³ĢÖŠĒāĘųµÄĪļÖŹµÄĮæ¼õŠ”£¬ĖµĆ÷·“Ó¦Ļņ×ÅÕżĻņŅĘ¶Æ£¬Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬
¹Ź“š°øĪŖ£ŗ“óÓŚ£»
£Ø2£©ÓÉĶ¼1æÉÖŖ£¬0”«1minÄŚĒāĘųµÄ±ä»ÆĮæĪŖ8mol-6mol=2mol£» B£®1”«3minÄŚĒāĘųµÄ±ä»ÆĮæĪŖ6mol-3mol=3mol£¬Ę½¾ł1min±ä»ÆĮæĪŖ1.5mol£» C£®3”«8minÄŚĒāĘųµÄ±ä»ÆĮæĪŖ3mol-2mol=1mol£¬Ę½¾ł1min±ä»ÆĮæĪŖ0.2mol£»D£®8”«11min“ļĘ½ŗāדĢ¬£¬ĒāĘųµÄĪļÖŹµÄĮæ²»ŌŁ±ä»Æ£®¹Ź1”«3minĖŁĀŹŌö“ó£¬8”«11minĖŁĀŹ×īŠ”£¬
¹Ź“š°øĪŖ£ŗA£»D£»
£Ø3£©ÓÉĶ¼ĻóæÉÖŖ£¬ŹµĻß±ķŹ¾µÄĒśĻߣ¬ŌŚ8·ÖÖÓ“ļµ½Ę½ŗāדĢ¬£¬“ĖŹ±ĒāĘųµÄĪļÖŹµÄĮæĪŖ2mol£¬ĒāĘųµÄÅضČĪŖ£ŗ2/2=1mol/LĒāĘųµÄÅØ¶Č±ä»ÆĪŖ£ŗ8/2¼õČ„1µČÓŚ3mol·“Ó¦Ē°¶žŃõ»ÆĢ¼µÄÅضČĪŖ£ŗ6/2=3mol/LĄūÓĆ»ÆŃ§Ę½ŗāµÄČż¶ĪŹ½æɵĆ,
CO2£Øg£©£«3H2£Øg£© CH3OH£Øg£©£«H2O£Øg£©
CH3OH£Øg£©£«H2O£Øg£©
ĘšŹ¼ĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 3 4 0 0
×Ŗ»ÆĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 1 3 1 1
Ę½ŗāĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 2 1 1 1 £Ø1·Ö£©
H2µÄ×Ŗ»ÆĀŹ=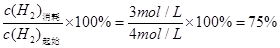 »ņ0.75
»ņ0.75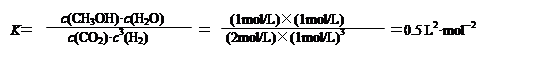
£Ø4£©¶ŌÓŚæÉÄę·“Ó¦CO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©”÷H=-49.0kJ?mol-1£¬Õż·“Ó¦ŹĒĢå»ż¼õŠ”µÄ·ÅČČ·“Ó¦£»ÓÉĶ¼1æÉÖŖ£¬ĒśĻߢń×īĻȵ½“ļĘ½ŗā£¬Ę½ŗāŹ±ĒāĘųµÄĪļÖŹµÄĮæŌö“󣬹ŹøıäĢõ¼žÓ¦Ōö“ó·“Ó¦ĖŁĀŹĒŅĘ½ŗāĻņÄę·“Ó¦ŅĘ¶Æ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ĪŖ£ŗÉżøßĪĀ¶Č£»ĒśĻߢņµ½“ļĘ½ŗāµÄŹ±¼ä±ČŌĘ½ŗā¶Ģ£¬Ę½ŗāŹ±ĒāĘųµÄĪļÖŹµÄĮæ¼õŠ”£¬¹ŹøıäĢõ¼žÓ¦Ōö“ó·“Ó¦ĖŁĀŹĒŅĘ½ŗāĻņÕż·“Ó¦ŅĘ¶Æ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ĪŖ£ŗŌö“óŃ¹Ēæ»ņÕߏĒŌö“óCO2ÅØ¶Č£¬
¹Ź“š°øĪŖ£ŗÉżøßĪĀ¶Č£»Ōö“óŃ¹Ē森
æ¼µć£ŗ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāĶ¼Ļ󔢷“Ó¦ĖŁĀŹ“óŠ”ÅŠ¶Ļ”¢Ķā½ēĢõ¼ž¶ŌĘ½ŗāµÄÓ°ĻģµČ


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĢśŗĶĻ”ĮņĖįŌŚ³ØæŚČŻĘ÷ÖŠ½ųŠŠ·“Ó¦£ŗ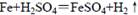 £¬ĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ
£¬ĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ
A£®øĆ·“Ó¦µÄ·“Ó¦¹ż³ĢÓėÄÜĮæ¹ŲĻµæÉŅŌÓĆĻĀĶ¼±ķŹ¾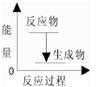 |
| B£®Čō½«øĆ·“Ó¦Éč¼Ę³ÉŌµē³Ų£¬µ±Õż¼«²śÉś22£®4LĘųĢåŹ±£¬ÓŠ56gĢśČܽā |
| C£®Čō½«øĆ·“Ó¦Éč¼Ę³ÉŌµē³Ų£¬ČÜŅŗÖŠSO42-ĻņFeµē¼«ŅĘ¶Æ |
| D£®Čō½«øĆ·“Ó¦Éč¼Ę³ÉŌµē³Ų£¬øŗ¼«·¢ÉśµÄ·“Ó¦ŹĒ£ŗFe -2e =Fe2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ¶Ō»Æѧ·“Ó¦µÄČĻŹ¶ÕżČ·µÄŹĒ
| A£®»Æѧ·“Ó¦±ŲČ»ŅżĘšĪļ֏דĢ¬µÄ±ä»Æ |
| B£®»Æѧ·“Ó¦Ņ»¶ØÓŠ»Æѧ¼üµÄ¶ĻĮŃŗĶÉś³É |
| C£®ŠčŅŖ¼ÓČȵķ“Ó¦Ņ»¶ØŹĒĪüČČ·“Ó¦ |
| D£®Čō·“Ó¦ĪļµÄ×ÜÄÜĮæøßÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬ŌņøĆ·“Ó¦ŹĒĪüČČ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖ298 K,101 kPaŹ±£¬2SO2(g)£«O2(g)  2SO3(g)£»¦¤H£½£197 kJ”¤mol£1”£ŌŚĻąĶ¬ĪĀ¶ČŗĶŃ¹ĒæĻĀ£¬ĻņĆܱÕČŻĘ÷ÖŠĶØČė2 mol SO2ŗĶ1 mol O2£¬“ļµ½Ę½ŗāŹ±£¬·Å³öČČĮæĪŖQ1£¬ĻņĮķŅ»øöĢå»żĻąĶ¬µÄČŻĘ÷ÖŠĶØČė1 mol SO2,0.5 mol O2ŗĶ1 mol SO3£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæĪŖQ2£¬ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ(””””)
2SO3(g)£»¦¤H£½£197 kJ”¤mol£1”£ŌŚĻąĶ¬ĪĀ¶ČŗĶŃ¹ĒæĻĀ£¬ĻņĆܱÕČŻĘ÷ÖŠĶØČė2 mol SO2ŗĶ1 mol O2£¬“ļµ½Ę½ŗāŹ±£¬·Å³öČČĮæĪŖQ1£¬ĻņĮķŅ»øöĢå»żĻąĶ¬µÄČŻĘ÷ÖŠĶØČė1 mol SO2,0.5 mol O2ŗĶ1 mol SO3£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæĪŖQ2£¬ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ(””””)
| A£®Q2£¼Q1£¼197 kJ”¤mol£1 | B£®Q2£½Q1£½197 kJ”¤mol£1 |
| C£®Q1£¼Q2£¼197 kJ”¤mol£1 | D£®Q2£½Q1£¼197 kJ”¤mol£1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖ·“Ó¦A£«B£½C£«DµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
| A£®øĆ·“Ó¦ĪŖĪüČČ·“Ó¦ |
| B£®AĪļÖŹÄÜĮæŅ»¶ØµĶÓŚCĪļÖŹÄÜĮæ |
| C£®øĆ·“Ó¦Ö»ÓŠŌŚ¼ÓČČĢõ¼žĻĀ²ÅÄܽųŠŠ |
| D£®·“Ó¦ĪļµÄ×ÜÄÜĮæøßÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
Ķ¬ĖŲŅģŠĪĢåĻą»„×Ŗ»ÆµÄ·“Ó¦ČČĻąµ±Š”¶ųĒŅ×Ŗ»ÆĖŁ¶Č½ĻĀż£¬ÓŠŹ±»¹ŗܲ»ĶźČ«£¬²ā¶Ø·“Ó¦ČČŗÜĄ§ÄŃ”£ĻÖŌŚæÉøł¾ŻøĒĖ¹Ģį³öµÄ¹Ūµć”°²»¹Ü»Æѧ¹ż³ĢŹĒŅ»²½Ķź³É»ņ·Ö¼ø²½Ķź³É£¬Õāøö×ܹż³ĢµÄČČŠ§Ó¦ŹĒĻąĶ¬µÄ”±Ą“ŃŠ¾æ”£ŅŃÖŖ£ŗ
¢ŁP4(s”¢°×Į×)£«5O2(g)=P4O10(s)£»¦¤ H=£2983.2 KJ”¤mol£1
¢ŚP(s”¢ŗģĮ×)£«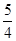 O2(g)=
O2(g)= P4O10(s)£»¦¤ H=£738.5KJ”¤mol£1
P4O10(s)£»¦¤ H=£738.5KJ”¤mol£1
ŹŌŠ“³ö°×Į××Ŗ»ÆĪŖŗģĮ×µÄČČ»Æѧ·½³ĢŹ½
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø12·Ö£©£Ø1£©“ÓÄÜĮæµÄ±ä»ÆŗĶ·“Ó¦µÄæģĀżµČ½Ē¶ČŃŠ¾æ·“Ó¦£ŗ2H2 + O2 = H2O”£ ŅŃÖŖøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ĻĀĶ¼ÄÜÕżČ·±ķŹ¾øĆ·“Ó¦ÖŠÄÜĮæ±ä»ÆµÄŹĒ________”£
“Ó¶Ļ¼üŗĶ³É¼üµÄ½Ē¶Č·ÖĪöÉĻŹö·“Ó¦ÖŠÄÜĮæµÄ±ä»Æ”£»Æѧ¼üµÄ¼üÄÜČēĻĀ±ķ£ŗ
| »Æѧ¼ü | H”ŖH | O£½O | H”ŖO |
| ¼üÄÜkJ/mol | 436 | 496 | 463 |
 xC(g)£¬·“Ó¦1minŹ±²āµĆŹ£Óą1.8molA£¬CµÄÅضČĪŖ0.4mol/L£¬Ōņ1minÄŚ£¬BµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ £»XĪŖ ”£Čō·“Ó¦¾2min“ļµ½Ę½ŗā£¬Ę½ŗāŹ±CµÄÅØ¶Č 0.8mol/L£ØĢī”°“óÓŚ£¬Š”ÓŚ»ņµČÓŚ”±£©”£ČōŅŃÖŖ“ļĘ½ŗāŹ±£¬øĆČŻĘ÷ÄŚ»ģŗĻĘųĢå×ÜŃ¹ĒæĪŖp£¬»ģŗĻĘųĢåĘšŹ¼Ń¹ĒæĪŖp0”£ĒėÓĆp0”¢pĄ“±ķŹ¾“ļĘ½ŗāŹ±·“Ó¦ĪļAµÄ×Ŗ»ÆĀŹĪŖ ”£
xC(g)£¬·“Ó¦1minŹ±²āµĆŹ£Óą1.8molA£¬CµÄÅضČĪŖ0.4mol/L£¬Ōņ1minÄŚ£¬BµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ £»XĪŖ ”£Čō·“Ó¦¾2min“ļµ½Ę½ŗā£¬Ę½ŗāŹ±CµÄÅØ¶Č 0.8mol/L£ØĢī”°“óÓŚ£¬Š”ÓŚ»ņµČÓŚ”±£©”£ČōŅŃÖŖ“ļĘ½ŗāŹ±£¬øĆČŻĘ÷ÄŚ»ģŗĻĘųĢå×ÜŃ¹ĒæĪŖp£¬»ģŗĻĘųĢåĘšŹ¼Ń¹ĒæĪŖp0”£ĒėÓĆp0”¢pĄ“±ķŹ¾“ļĘ½ŗāŹ±·“Ó¦ĪļAµÄ×Ŗ»ÆĀŹĪŖ ”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø3·Ö£©æĘѧ¼ŅŅ»Ö±ÖĀĮ¦ÓŚ”°ČĖ¹¤¹ĢµŖ”± µÄ·½·ØŃŠ¾æ”£ÄæĒ°ŗĻ³É°±µÄ¼¼ŹõŌĄķĪŖµŖĘųŗĶĒāĘųŌŚøßĪĀøßŃ¹“߻ƼĮĢõ¼žĻĀÉś³É°±Ęų£¬Ņ»¶ØĢõ¼žĻĀ£¬ĻņŅ»øö1LµÄĆܱÕČŻĘ÷ÖŠ³äČė2molN2ŗĶ6molH2£¬·“Ó¦“ļĘ½ŗāŹ±Éś³ÉNH3µÄÅضČĪŖ1 mol”¤L-1£¬²¢·Å³öQ kJČČĮ棬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ ____ __”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø14·Ö£©¶ž¼×ĆŃ£ØCH3OCH3£©ŗĶ¼×“¼£ØCH3OH£©¶¼ŹĒøߊ§Ēå½ąÄÜŌ“”£¹¤ŅµÉĻĄūÓĆĆŗµÄĘų»Æ²śĪļ£ØĖ®ĆŗĘų£©ŗĻ³É¼×“¼ŗĶ¶ž¼×ĆŃ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Öʱø¶ž¼×ĆŃ×īŗóŅ»²½·“Ó¦ÓÉAl2O3“߻Ƽד¼ĶŃĖ®ŗĻ³É£¬·“Ó¦·½³ĢŹ½ĪŖ ”£
£Ø2£©ŅŃÖŖ£ŗCO(g)+2H2(g)=CH3OH (g) ”÷H= ”Ŗ90.1kJ”¤mol-1 CO(g)µÄČ¼ÉÕČČŹĒ282.8 kJ”¤mol-1£»H2µÄČ¼ÉÕČČŹĒ285.8 kJ”¤mol-1Š“³ö±ķŹ¾CH3OH (g) Č¼ÉÕČȵÄČČ»Æѧ·“Ó¦·½³ĢŹ½ ”£
£Ø3£©¶ž¼×ĆŃÖ±½ÓČ¼ĮĻµē³Ų±Č¼×“¼Ö±½ÓČ¼ĮĻµē³Ųøüøߊ§£¬µČÖŹĮæµÄ¶ž¼×ĆŃŗĶ¼×“¼ĶźČ«·Åµē×ŖŅʵē×ÓµÄĪļÖŹµÄĮæÖ®±ČŹĒ ”£Óƶž¼×ĆŃÖ±½ÓČ¼ĮĻµē³Ųµē½ā×ćĮ汄ŗĶŹ³ŃĪĖ®£¬µ±ĻūŗÄ9.2g¶ž¼×ĆŃŹ±ĄķĀŪÉĻŅõ¼«²śÉśµÄĘųĢåµÄĢå»żĪŖ L”££Ø±źæöĻĀ£©
£Ø4£©ŌŚŗĻ³ÉÖŠ°éÓŠĖ®ĆŗĘų½»»»·“Ó¦£ŗCO(g)+H2O(g)  CO2(g)+H2(g)£¬µČĪļÖŹµÄĮæµÄCO(g)ŗĶH2O(g)¼ÓČėĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬Ę½ŗāŹ±²āµĆ½į¹ūČēĻĀ±ķ”£
CO2(g)+H2(g)£¬µČĪļÖŹµÄĮæµÄCO(g)ŗĶH2O(g)¼ÓČėĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬Ę½ŗāŹ±²āµĆ½į¹ūČēĻĀ±ķ”£
| ĪĀ¶Č | 260”ę | 280”ę | 295”ę | 310”ę |
| CO×Ŗ»ÆĀŹ | 89% | 80% | 75% | 60% |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com