
现有温度相同、pH=a和pH=b的两种NaOH溶液,已知b=a+2,将两种溶液等体积混合后,所得溶液的pH接近于
A.a-lg2 B.b-lg2 C.a+lg2 D.b+lg2
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g) 2NH3(g)△H=﹣92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=﹣92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:
容器 编号 | 起始时各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述不正确的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15kJ
D.若容器①体积为0.5L,则平衡时放出的热量小于23.15kJ
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考二化学卷(解析版) 题型:选择题
己知在碱性溶液中可发生如下反应:2R(OH)3+3ClO-+4OH-==2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是
A.+3 B.+4 C.+5 D.+6
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考二化学卷(解析版) 题型:选择题
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O═H2SO4+2HBr相比较,水的作用不相同的是
A.2Al+2NaOH+2H2O═2NaAlO2+3H2↑
B.4Fe(OH)2+O2+2H2O═4Fe(OH)3
C.BrCl+H2O=HCl+HBrO
D.2Na2O2+2H2O═4NaOH+O2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:填空题
如图所示,有T1、T2两种温度下BaSO4在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:

(1)T1________T2(填“>”、“<”或“=”),T2温度时时Ksp(BaSO4)=___________。
(2)根据T1温度时BaSO4的沉淀溶解平衡曲线,判断下列说法正确的是________(填序号)。
A.加入Na2SO4可由a点变为b点
B.在T1曲线上方区域(不含曲线)的任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能由d点变为T1曲线上a、b之间的某一点(不含a、b)
D.升温可由b点变为d点
(3)T2时, 现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理.若使BaSO4中的SO42-全部转化到溶液中,需要反复处理________次。[提示:BaSO4(s)+CO32-(aq)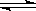 BaCO3(s)+SO42- (aq),K= Ksp(BaSO4/ Ksp(BaCO3);Ksp(BaCO3)=1.19×10-7]
BaCO3(s)+SO42- (aq),K= Ksp(BaSO4/ Ksp(BaCO3);Ksp(BaCO3)=1.19×10-7]
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:选择题
下列有关问题,与盐的水解有关的是
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
A.①②③ B.②③④ C.①④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:选择题
下列电解质溶液的有关叙述正确的是
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7+ G4 D* e% P% b
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)= c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上期中理化学卷(解析版) 题型:填空题
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识的回答:
(1)浓度为0.1mol/L的8种溶液:①HNO3 ②H2SO4 ③HCOOH ④Ba(OH)2 ⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl 溶液pH值由小到大的顺序是(填写编号)____________。
(2)B为0.1mol•L-1NaHCO3溶液,实验测得NaHCO3溶液的pH>7,请用离子方程式表示其原因:___________________。
(3)在0.10 mol•L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=___________(已知Ksp[Cu(OH) 2]=2.2x10-20)。若在0.10 mol•L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团二师华山中学高一期中化学卷(解析版) 题型:填空题
(1)用下列物质的编号填空:
①NaCl晶体 ②盐酸 ③HCl ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧稀硫酸 ⑨KOH溶液;
以上物质中属于电解质的是___________,属于非电解质的是___________,能导电的是___________。
(2)某烧杯中盛有100 mLHCl和CuCl2的混合液 ,混合溶液中c(HCl)=2 mol/L,c(CuCl2)=1 mol/L。请回答下列问题:
,混合溶液中c(HCl)=2 mol/L,c(CuCl2)=1 mol/L。请回答下列问题:
①该混合溶液中,n(H+)=________mol;c(Cl-)=__________mol/L。
向上述烧杯中加入足量铁粉并使之充分反应。写出有关的离子方程式:
② ; 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com