
【题目】Be(OH)2是两性的,跟强酸反应时生成Be2+ , 跟强碱反应时生成BeO22﹣ . 现有三份等物质的量浓度、等体积的BeCl2、MgCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mol)的关系如图所示,则与BeCl2、MgCl2、AlCl3三种溶液对应的图象正确的是( ) 
A.⑤③①
B.②③④
C.③⑤④
D.③②①
【答案】A
【解析】解:向氯化镁中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化镁,当氢氧化钠过量时,沉淀也不会溶解,量保持不变,故对应的是图象③;
向氯化铍溶液中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化锌,当氢氧化钠过量时,沉淀会溶解,依次发生反应BeCl2+2NaOH=Be(OH)2↓+2NaCl,Be(OH)2↓+2NaOH=Na2BeO2+2H2O,沉淀量达到最大和沉淀完全消失所消耗的氢氧化钠是相等的,故图象⑤是正确的,
向氯化铝溶液中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化铝,当氢氧化钠过量时,沉淀会溶解,依次发生反应:
AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3↓+NaOH=NaAlO2+2H2O,沉淀量达到最大和沉淀完全消失所消耗的氢氧化钠的物质的量之比是3:1,故图象①是正确的.则与BeCl2、MgCl2、AlCl3三种溶液对应的图象正确的是⑤③①;故A正确;
故选A.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型(如图),据此回答下列问题: 
(1)常温下含氢量最高的气态烃是(填字母).
(2)G的名称是
(3)能够发生加成的烃有种.
(4)一卤代物种类最多的是(填字母).
(5)写出实验室制D的化学方程式: .
(6)写出F发生硝化反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某火力发电厂使用的燃料煤中硫的质量分数为0.32%.该电厂每天要燃烧这种煤200t,请通过计算回答:
(1)如果煤中的硫全部转化为SO2 , 该电厂每天燃烧产生SO2多少升(标准状况)?
(2)将SO2用“钙基固硫法”处理可以“变废为宝”:SO2 ![]() CaSO3
CaSO3 ![]() CaSO4假设转化过程的损失可以忽略不计,计算该电厂每天用“钙基固硫法”处理产生的SO2 , 可获得纯度为85%的CaSO4多少吨?
CaSO4假设转化过程的损失可以忽略不计,计算该电厂每天用“钙基固硫法”处理产生的SO2 , 可获得纯度为85%的CaSO4多少吨?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产玻璃会产生大量的窑炉气(含SO2和氮氧化物等).为减少环境污染,某工厂生产玻璃与处理窑炉气的工艺流程如下: 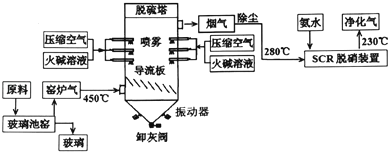
(1)生产普通硅酸盐玻璃的主要原料是石英砂、 和石灰石。其中,石灰石参与的反应方程式是 。
(2)窑炉气中的SO2一部分来源于原料中添加剂Na2SO4的热分解,该反应方程式为 ;氮氧化物主要源于空气中N2与O2的反应,该类气体在高温下基本无色,随温度的降低逐渐偏向红棕色,原因是 。
(3)“脱硫塔”中反应形成的灰分,除亚硫酸钠和氮的含氧酸盐外,主要还有 ;用于喷雾的火碱溶液应选用软化水配制,原因是 。
(4)在“脱硝装置”中,催化剂设计成蜂窝而韭平板状结构.原因是 。氧气在脱硝过程中的作用是
(5)净化气的主要成分是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下题:
(1)按系统命名法命名:
①有机物CH3CH(C2H5)CH(CH3)2的名称是。
(2)写出下列各种有机物的结构简式:
①2,3-二甲基-4-乙基己烷;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种烷烃,它们的分子式都是C8H18。
(1)A不能由任何分子式为C8H16的异构体加H2得到,A的结构简式为。
(2)B可以而且只能由一种分子式为C8H16的物质加H2得到,B的结构简式为。
(3)C可以而且只能由两种分子式为C8H16的物质D或E加H2得到,C的结构简式为 , D和E的结构简式分别为和。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过碳酸钠(2Na2CO33H2O2 )是由Na2CO3﹣与H2O2复合而形成的一种固体放氧剂,可用于洗涤、纺织、医药、卫生等领域.工业上常以过碳酸钠产品中活性氧含量([O]%= ![]() ×100)来衡量其优劣,13%以上为优等品.一种制备过碳酸钠的工艺流程如图1:
×100)来衡量其优劣,13%以上为优等品.一种制备过碳酸钠的工艺流程如图1: 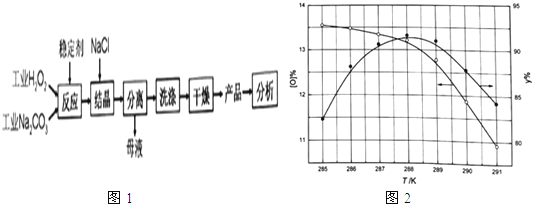
回答下列问题:
(1)过碳酸钠受热易分解,写出反应的化学方程式 .
(2)稳定剂及反应温度等因素对产品质量有很大影响.
①下列试剂中,可能用作“稳定剂”的是(填字母).a.MnO2b.KI c.Na2SiO3d.FeCl3
②反应温度对产品产率(y%)及活性氧含量的影响如图1所示.要使产品达到优等品且产率超过90%合适的反应温度范围是 .
③“结晶”时加入NaCl的目的是 , 其作用原理是 .
(3)“母液”中可循环利用的主要物质是 .
(4)产品中活性氧含量的测定方法:称量0.1600g样品,在250mL锥形瓶中用100mL 0.5molL﹣1硫酸溶解完全,立即用0.02000molL﹣1高锰酸钾标准溶液滴定,至溶液呈浅红色且半分钟内不褪色即为终点,平行三次,消耗KMnO4溶液的平均体积为26.56mLo另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMn04溶液的平均体积为2.24mL.
①过碳酸钠与硫酸反应,产物除硫酸钠和水外,还有 .
②测定时,若用工业盐酸代替硫酸,分析对测定结果的影响及其原因 .
③该样品的活性氧含量为%,表明该样品(填“是”或“不是”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com