
| A、2.7g | B、3.6g |
| C、5.04g | D、4.05g |
| 0.3mol×3 |
| 6 |
| 3 |
| 2 |
| 0.225mol×2 |
| 3 |


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
| A、X2+2Y2═2XY2 |
| B、2X2+Y2═2X2Y |
| C、3X2+Y2═2X3Y |
| D、X2+3Y2═2XY3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
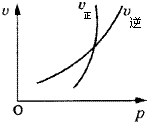
| A、N2O3(g)?NO2(g)+NO(g); 恒容时加入N2O3,平衡正向移动 |
| B、N2(g)+3H2(g)?2NH3(g); 将氨气液化分离后,有利于加快正反应速率 |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g); 加大氧气浓度,能提高氨气平衡转化率 |
| D、2SO2(g)+O2(g)?2SO3(g); 增大压强,平衡常数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、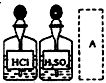 |
B、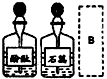 |
C、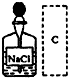 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 异常情况 | 可能的原因 |
| ① | 蒸发结晶时,蒸发皿破裂 | 将溶液蒸干或酒精灯灯芯碰到蒸发皿底部 |
| ② | 分液时,分液漏斗中的液体很难滴下 | 没有打开分液漏斗颈上的玻璃塞或塞上的凹槽与漏斗上的小孔没有对齐 |
| ③ | 萃取时,振荡溶液,静置不分层 | 萃取剂加得太多 |
| ④ | 蒸馏时,发现冷凝管破裂 | 没有通冷凝水或先加热后通冷凝水 |
| A、① | B、② | C、③ | D、④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com