
【题目】以下是氮循环的一部分: 
(1)通常状况下,NO2的颜色是;
(2)反应①的化学方程式是;
(3)NO2易溶于水,并和水发生化学反应.该反应中,氧化剂是;
(4)化合物A的化学式是;
(5)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:2NO+2CO═2CO2+N2 . 当生成2mol N2时,被还原的NO为mol.
【答案】
(1)红棕
(2)N2+O2 ![]() 2NO
2NO
(3)NO2
(4)HNO3
(5)4
【解析】解:(1)NO2是红棕气体,所以答案是:红棕;(2)氮气和氧气放电生成一氧化氮,反应为:N2+O2 ![]() 2NO,所以答案是:N2+O2
2NO,所以答案是:N2+O2 ![]() 2NO;(3)二氧化氮可以和水之间反应生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,化合价降低N元素所在的反应物NO2是氧化剂,所以答案是:NO2;(4)二氧化氮可以和水之间反应生成硝酸和一氧化氮,即3NO2+H2O=2HNO3+NO,化合物A的化学式是HNO3 , 所以答案是:HNO3;(5)反应2NO+2CO=2CO2+N2中,NO是氧化剂,被还原,生成氮气1mol,被还原的NO为2mol,所以当生成2mol N2时,被还原的NO为4mol,所以答案是:4.
2NO;(3)二氧化氮可以和水之间反应生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,化合价降低N元素所在的反应物NO2是氧化剂,所以答案是:NO2;(4)二氧化氮可以和水之间反应生成硝酸和一氧化氮,即3NO2+H2O=2HNO3+NO,化合物A的化学式是HNO3 , 所以答案是:HNO3;(5)反应2NO+2CO=2CO2+N2中,NO是氧化剂,被还原,生成氮气1mol,被还原的NO为2mol,所以当生成2mol N2时,被还原的NO为4mol,所以答案是:4.


科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铝合金投入100mL一定物质的量浓度盐酸中,合金全部溶解,向所得溶液中滴加4mol /LNaOH溶液至过量,生成沉淀的质量与加入NaOH溶液的体积关系如图(横坐标体积单位是mL,纵坐标质量单位是g),求:
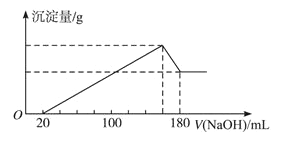
(1)原合金中Mg、Al质量各多少克?_________
(2)盐酸的物质的量浓度c(HCl)=____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能说明SO2具有漂白作用的是
A.SO2气体能使溴水褪色
B.SO2能使酸性高锰酸钾溶液褪色
C.SO2气体能使含NaOH的酚酞溶液褪色
D.SO2气体能使黄色的草帽辫变白色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应H2(g)+I2(g)2HI(g),0~5min内H2的浓度减少了0.1mol/L,则在这段时间内
用HI表示的平均反应速率为( )
A.0.01molL﹣1min﹣1
B.0.04molL﹣1min﹣1
C.0.2molL﹣1min﹣1
D.0.5molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把4.48LCO2通过一定量的固体过氧化钠后收集到3.36L气体(气体的测量均在标准状况下),所得气体的总质量是
A. 3.2g B. 4.8g C. 5.4g D. 6g
【答案】D
【解析】令参加反应的CO2气体的体积为a,生成的O2的体积为b,则:
2CO2+2Na2O2=2Na2CO3+O2↑,气体体积减小△V
2 1 1
a b 4.48L-3.36L=1.12L
解得:a=2.24L,b=1.12L,
生成氧气的体积1.12L,小于3.36L,故二氧化碳有剩余,
所以:3.36L气体中CO2体积为4.48L-2.24L=2.24L,O2的体积为1.12L,
所以4.48L气体的质量为![]() ×44g/mol+
×44g/mol+![]() ×32g/mol=6.0g。答案选D。
×32g/mol=6.0g。答案选D。
点睛:本题考查根据方程式的计算,难度中等,本题采取差量法计算,可以避免单独讨论或计算判断最后气体的组成,注意差量法的理解与运用。根据气体的体积差,通过差量法计算参加反应的二氧化碳体积、生成的氧气的体积,判断3.36L气体的组成及各成分的体积,再根据n=![]() 计算各组分气体的物质的量,利用m=nM计算质量。
计算各组分气体的物质的量,利用m=nM计算质量。
【题型】单选题
【结束】
26
【题目】某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。请回答下列问题。
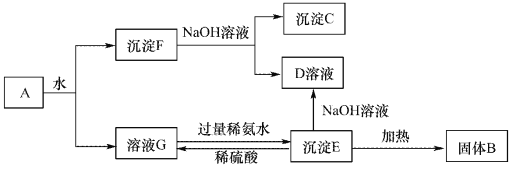
(1)沉淀F与NaOH溶液反应的离了方程式为_______________。
(2)沉淀C与稀硫酸反应的离子方程式为_______________。
(3)溶液G与过量稀氨水反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制取氨气并完成喷泉实验(图中夹持装置均已略去). 
(1)写出实验室制取氨气的化学方程式 .
(2)收集氨气应使用法,要得到干燥的氨气可选用作干燥剂.
(3)用图Ⅰ所示装置进行喷泉实验,上部烧瓶已装满干燥的氨气,引发喷泉的操作是 , 该实验的原理是 .
(4)如果只提供如图Ⅱ所示装置,请说明引发喷泉的方法是
(5)写出氨气催化氧化的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在MgCl2和AlCl3的混合液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。
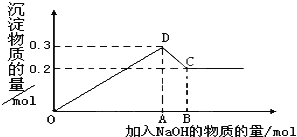
(1)写出下列线段内发生反应的方程式:
OD段__________________________________。
CD段__________________________________。
(2)图中C点表示加入________mol NaOH时。
(3)原溶液中来自MgCl2、AlCl3 的氯离子物质的量浓度之比为_____________。
(4)图中线段OB:OA=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就三大酸与金属反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解.该反应的化学方程式为: .
(2)在一定体积的10molL﹣1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol.则浓硫酸的实际体积(填“大于”、“等于”或“小于”)180mL.若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为 .
(3)欲迅速除去铝壶底部的水垢,又不损坏铝壶,最好的方法是
A.浓盐酸
B.稀硝酸
C.冷的浓硝酸
D.冷的浓硫酸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用稀盐酸与稀NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 
(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和 . 泡沫塑料的作用是 .
(2)若NaOH溶液用相同浓度和体积的下列溶液代替,则对中和热数值测定结果将如何影响(填“偏大”、“偏小”、“无影响”):KOH溶液;氨水(NH3H2O) .
(3)某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).由题干及图形可知,V1:V2=时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com