
分析 (1)恒温恒容下,气体的压强与气体体积成正比,测得平衡时容器内气体的压强比反应前小,说明是体积减小的反应;x只能为1;
(2)根据化学平衡常数概念得表达式;
(3)根据三段式可得平衡时的各物质的浓度;
(4)根据反应速率v=$\frac{△c}{△t}$计算.
解答 解:(1)恒温恒容下,气体的压强与气体体积成正比,测得平衡时容器内气体的压强是反应前的$\frac{5}{6}$,说明平衡时容器内气体的压强比反应前小,说明是体积减小的反应,x只能为1;
故答案为:1
(2)化学平衡常数为生成物的浓度幂之积与反应物浓幂之积,则k=$\frac{c(C)•{c}^{2}(D)}{{c}^{3}(A)•c(B)}$;
故答案为:$K=\frac{{c(C)•{c^2}(D)}}{{{c^3}(A)•c(B)}}$
(3)设反应A3amol,根据三段式:
3A(g)+B(g)?C(g)+2D(g)
起始量:2 1 0 0
转化量:3a a a 2a
平衡量:2-3a 1-a a 2a
则有:$\frac{2-3a+1-a+a+2a}{2+1}$=$\frac{5}{6}$,得a=0.5mol,所以平衡时a的浓度为:$\frac{(2-3×0.5)mol}{10L}$=0.05mol/L;
故答案为:0.05
(4)B的反应速率为:$\frac{0.5mol÷10L}{2min}$=0.025mol.L-1.min-1;
故答案为:0.025mol.L-1.min-1
点评 本题考查了化学平衡计算的分析应用,主要是反应速率、转化率、平衡常数的概念计算,掌握基础是关键,题目难度中等,注意速率的单位.


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:选择题
| A. | c(Ba2+)浓度增大 | B. | 溶液中Ba2+数目减少 | ||
| C. | 溶液pH减小 | D. | 溶液pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
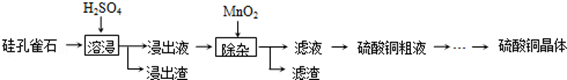
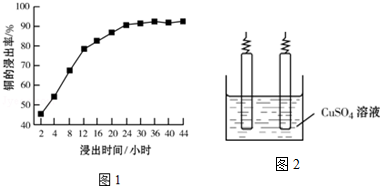
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
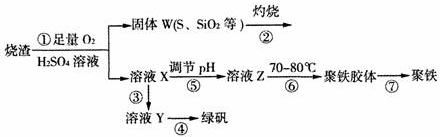
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
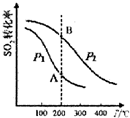 研究硫酸工业原理及含硫化合物的性质具有重要意义.
研究硫酸工业原理及含硫化合物的性质具有重要意义.| 气体 | SO2 | O2 | SO3 |
| 浓度(mol•L-1) | 0.4 | 1.2 | 1.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
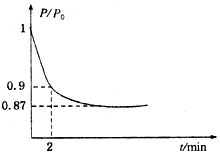 能源的开发利用与人类社会的可持续性发展息息相关.
能源的开发利用与人类社会的可持续性发展息息相关.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | M与A均能使酸性高锰酸钾溶液和溴水褪色 | |
| B. | B中含有羧基和羟基两种官能团,B能发生消去反应和酯化反应 | |
| C. | 1molM与热的烧碱溶液反应,可消耗2nmol的NaOH | |
| D. | A、B、C各1mol分别与金属钠反应,放出气体的物质的量之比为1:2:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com