
【题目】三种正盐的混合溶液中含有0.2molK+、0.25molZn2+、0.4molCl- 和SO42-,则SO42-的物质的量为
A. 0.15mol B. 0.1mol
C. 0.3mol D. 0.5mol
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】(NH4)2Fe(SO4)2·6H2O俗称莫尔盐,浅绿色晶体,是化学定量分析中的常用试剂。其分解情况复杂,某课题组通过实验检验莫尔盐隔绝空气加热时的分解产物。
⑴分解装置A应选用_________(填“①”或“②”)。


① ②
⑵若实验中A装置中的固体变为红棕色,则固体产物中含有_____;C装置中红色褪去,说明气体产物中含有______;C装置后应连装置D(未画出),其作用是_______。
⑶若想利用上述装置证明分解产物中含有氨气,只需更换B、C中的试剂即可,则更换后的试剂为B_____________、C______________(填序号)。
①碱石灰 ②无水氯化钙 ③酚酞溶液 ④稀硫酸
⑷某同学认为莫尔盐分解还可能会生成N2、SO3,拟从下列装置中选择合适的装置加以证明,则正确的连接顺序是A、_____、_____、E,反应一段时间后,再接_______。

⑸若实验证实(2)(3)的猜想是正确的,(4)中的气体产物只有一种,另外只有水生成,则据此推测的莫尔盐分解反应的化学方程式可能为 ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是:
A. Cl2通往NaOH溶液中:Cl2+OH-=Cl-+ClO-+H2O
B. NaHCO3溶液中加入HCl:CO32-+2H+=CO2↑+H2O
C. AlCl3溶液中加入过量稀氨水:Al3++4NH3H2O =AlO2-+4NH4++2H2O
D. Cu溶液于稀HNO3:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量金属钠投入到氯化铁溶液中,产物是
A. Fe(OH)3、NaCl,H2
B. Fe,NaCl
C. NaOH、H2
D. H2、NaCl、NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员以Zn和尖晶石型锰酸锌(ZnMn2O4)为电极材料,研制出一种水系锌离子电池。该电池的总反应方程式:xZn + Zn1xMn2O4![]() ZnMn2O4(0 < x < 1)。下列说法正确的是
ZnMn2O4(0 < x < 1)。下列说法正确的是
A. 充电时,Zn2+向ZnMn2O4电极迁移
B. 充电时,阳极反应:ZnMn2O4 2xe—=Zn1-xMn2O4+xZn2+
C. 放电时,每转移1mol e-,ZnMn2O4电极质量增加65g
D. 充放电过程中,只有Zn元素的化合价发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现需要0.1 mol·L1CuSO4溶液240 mL,实验室提供以下试剂用于溶液的配制:蒸馏水、胆矾晶体(CuSO4·5H2O)、4 mol·L1CuSO4溶液
(1)无论采用何种试剂进行配制,除烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是_________,在使用该仪器前必须进行的操作是___________。
(2)若用胆矾晶体进行配制,需用托盘天平称取CuSO4·5H2O的质量为_______ g;如果用 4 mol/L的CuSO4溶液稀释配制,需用量筒量取________mL 4 mol/LCuSO4溶液。
(3)用4 mol/L的硫酸铜溶液稀释配制溶液所需的实验步骤有:
a.用量筒量取一定体积4 mol/L的硫酸铜溶液于一烧杯中
b.洗涤烧杯和玻璃棒2~3次并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
c.计算所需4 mol/L硫酸铜溶液的体积
d.盖好瓶塞,反复上下颠倒摇匀后,将溶液转存于试剂瓶中
e.加水至液面离容量瓶刻度线1~2 cm处改用胶头滴管进行定容
f.往烧杯中加入约100 mL水进行初步稀释,冷却至室温
g.将溶液转移入容量瓶
其中正确的操作顺序为______________________。
(4)下列操作对所配制溶液浓度的影响(填“偏高”“偏低”或“无影响”)。
①称取的胆矾晶体失去了部分结晶水___________。
②定容时,仰视刻度线:___________。
③容量瓶未干燥,有少量蒸馏水:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对烟道气中的SO2进行回收再利用具有较高的社会价值和经济价值。
Ⅰ. CO还原法
(1)一定条件下,由SO2和CO反应生成S和CO2的能量变化如右图I所示,每生成16gS(s) ,该反应_______(填“放出”或“吸收”)的热量为_________。

(2)在绝热恒容的密闭容器中,进行反应:
2CO(g)+SO2(g) ![]() S(s)+2CO2(g),该反应的平衡常数表达式为_______。对此反应下列说法正确的是__________
S(s)+2CO2(g),该反应的平衡常数表达式为_______。对此反应下列说法正确的是__________
A.若混合气体密度保持不变,则已达平衡状态
B.反应开始到平衡时,容器内气体的压强保持不变
C.达平衡后若再充人一定量CO2,平衡常数保持不变
D.分离出S,正、逆反应速率均保持不变
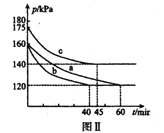
(3)向2L恒温恒容密闭容器中通入2molCO和lmolSO2,分别进行a、b、c三组实验。在不同条件下发生反应:2CO(g)+SO2(g)![]() S(s)+2CO2,反应体系总压强随时间的变化曲线如下图Ⅱ所示,则三组实验温度的关系是a ______b ______c (填“> ”、“< ”、或“=”) ;实验a从反应开始至平衡时,反应速率v(SO2)=____________。
S(s)+2CO2,反应体系总压强随时间的变化曲线如下图Ⅱ所示,则三组实验温度的关系是a ______b ______c (填“> ”、“< ”、或“=”) ;实验a从反应开始至平衡时,反应速率v(SO2)=____________。
Ⅱ.Na2SO3溶液吸收法
常温下,用300mL1.0mol·L-1,Na2SO3溶液吸收SO2的过程中,溶液pH随吸收SO2物质的量的变化曲线如上图Ⅲ所示。
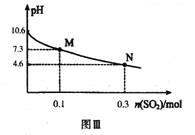
(4)1.0mol·L-1 Na2SO3溶液中离子浓度由大到小的顺序为_________
(5)若用等体积、等物质的量浓度的下列溶液分别吸收SO2,则理论上吸收量最多的是____
A. NH3·H2O B. Na2S C. Na2CO3 D. FeCl3
(6)常温下,H2SO3的二级电离平衡常数Ka2的数值为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年12月6日,上海遭遇重度雾霾,空气质量指数达六级重度污染。雾霾是雾和霾的混合物,其中雾是自然天气现象,霾的核心物质是悬浮在空气中的烟、灰尘等物质,其中霾属于悬浊液,雾所属的分散系是( )
A. 溶液 B. 悬浊液 C. 乳浊液 D. 胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com