
下列离子方程式正确的是
A. 氯气溶于水:Cl2+H2O 2H++ClO-+Cl-
2H++ClO-+Cl-
B. 亚硫酸钠溶液被空气中的氧气氧化:SO32-+O2=SO42-
C. 氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
D. 碳酸氢铵溶液和足量的氢氧化钠溶液混合加热:NH4++HCO3-+2OH-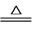 NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O
科目:高中化学 来源:2016-2017学年河北省张家口市高一上学期期末考试化学试卷(解析版) 题型:选择题
将Cl2通入200mL0.5mol·L-1氢氧化钾溶液中,二者恰好完全反应得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量之比是1︰2,则通入的Cl2在标准状况下的体积为
A. 0.56L B. 1.68L C. 2.24L D. 1.12L
查看答案和解析>>
科目:高中化学 来源:2017届山西省名校高三下学期联考理综化学试卷(解析版) 题型:简答题
人口资源环境委员会副主任、中国科学院院士秦大河表示,当前情况下散烧煤和没有清洁的煤是造成中国城市雾霾或者东部雾霾的主要原因。煤的气化是解决雾霾,清洁地利用煤炭的重要途径之一。
⑴已知:H2O(g)=H2O(I) △H=-44kJ/mol
物质 | H2(g) | C(s) | CO(g) |
燃烧热kJ/mol | -285.8 | -393.5 | -283.0 |
①请写出煤的气化反应生成合成气(CO和H2)的热化学方程式___________。
②在恒温、恒容的反应器中,能表明上述反应达到平衡状态的是_______。
a.混合气体平均相对分子质量不再改变
b.气体压强不再改变
c.各气体浓度相等
d.反应体系中温度保持不变
e.断裂氢氧键速率是断裂氢氢键速率的2倍
f.混合气体密度不变
g.单位时间内,消耗水的质量与生成氢气的质量比为9:1
⑵在催化剂作用下合成气合成甲烷过程中会发生如下反应:
I CO(g)+3H2(g) = CH4(g)+H2O(g) △H1= -206 kJ/mol
II CO(g)+H2O(g) = CO2(g)+H2(g) △H2= -41 kJ/mol
Ⅲ 2CO(g)+2H2(g)= CH4(g)+CO2(g) △H 3= -247.4 kJ/mol
①图1是太原理工大学煤化工研究所利用热力学数据分析得到温度对反应ⅠInK(化学平衡常数K的自然对数)的曲线图,请分析出现这样趋势的原因是____________。
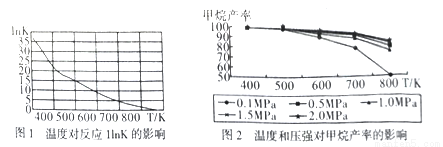
②提高甲烷反应选择性的关键因素是_______,根据相关知识和图2分析合成甲烷适宜的反应条件是
在550~630K,1MPa的原因是__________________。
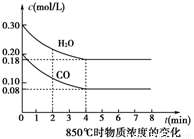
③850℃时在体积为5L反应器中发生反应Ⅱ,CO和H2O(g)浓度变化如图所示,请列式计算此条件下的平衡常数_____________ 。
(3)CH4燃料电池利用率很高,装置中添加1L2mol/L的KOH溶液为电解质,持续缓慢通入标准状况下甲烷22.4L~33.6 L时负极电极反应为___________。
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:选择题
已知还原性:SO32->I-。某溶液X可能含有NH4+、Na+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,为确定其组成,某同学进行如下实验:
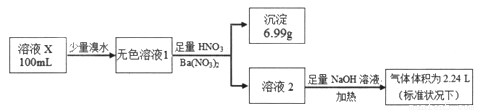
下列说法正确的是
A. 溶液X肯定只存在NH4+、SO42-
B. 溶液X一定不含有Ba2+、Fe3+,可能含有I-
C. 为确定可能存在的阴离子,可另取试液滴加足量盐酸、BaCl2溶液
D. 为确定可能存在的阳离子,可用经过稀硫酸洗过的铂丝蘸取溶液X在酒精灯火焰上灼烧
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:选择题
下列说法不正确的是
A. NH4Cl溶液呈酸性说明NH3·H2O是弱电解质
B. 醋酸钠溶液中c(Na+)>c(CH3COO-)
C. 常温下相同pH的NaOH溶液和CH3COONa溶液中水电离出的OH-浓度相同
D. 常温下,在1mol·L-1的盐酸中加入等体积等浓度的氨水,溶液导电能力减弱
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:选择题
下列有关铁、铜及其化合物的说法正确的是
A. 铁和铜在自然界中主要以游离态的形式存在
B. 工业上在高温下用CO还原含Fe2O3的铁矿石炼铁
C. 常温下铁与浓硫酸不反应
D. 用激光照射硫酸铜溶液可观察到丁达尔现象
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:选择题
下列物质属于碱性氧化物的是
A. SiO2 B. CaO C. CO D. NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:选择题
设NA代表阿伏加德罗常数,下列说法正确的是
A. 24g金属镁变为镁离子时失去的电子数为NA
B. 18g水所含的电子数目为NA
C. 在常温常压下11.2L二氧化硫所含的分子数目为0.5NA
D. 在常温常压下32g氧气所含的原子数目为2NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
2FeS + 6H2SO4(浓) = Fe2(SO4)3 + 2 S ↓ + 3SO2 ↑ + 6H2O ,下列说法正确的是( )
A. 反应中氧化产物为Fe2(SO4)3和SO2
B. 氧化剂和还原剂的物质的量之比为3:1
C. 反应中每产生32g沉淀转移电子的数目为2NA
D. 反应中被Fe还原的硫酸和被S还原的硫酸之比1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com