

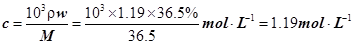 。(2) A、溶液中HCl的物质的量=nV,所以与溶液的体积有关,A不合题意;B、溶液的浓度
。(2) A、溶液中HCl的物质的量=nV,所以与溶液的体积有关,A不合题意;B、溶液的浓度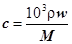 ,与溶液的体积无关,B符合题意;C、溶液中Cl–的数目=nNA=cVNA,所以与溶液的体积有关,C不合题意;D、溶液的密度与溶液的体积无关,D符合题意;答案为BD。(3)①设需要量取的浓盐酸的体积为V,则11.9mol·L–1×V=0.5L×0.400mol·L–1,V=0.0168L=16.8mL,故答案为16.8;②配制溶液时除烧杯和玻璃棒,还需要的仪器有量筒、500mL容量瓶、胶头滴管;③实验开始时,需要检查容量瓶是否漏水;④配制溶液时,操作步骤为:称量→溶解→冷却→转移→洗涤→定容→摇匀,故答案为:FCEGABD;⑤Ⅰ、用量筒量取浓盐酸时俯视观察凹液面,则所取浓盐酸的体积偏小,所配溶液的浓度偏小;Ⅱ、定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水,溶液的体积偏大,所以配制溶液的浓度偏小;Ⅲ、配制时,容量瓶有少量蒸馏水,不会影响溶液体积,也不会影响所配溶液中溶质的物质的量,所以不会影响溶液浓度;Ⅳ、定容时仰视刻度线,则溶液的体积偏大,配得的溶液浓度偏小。
,与溶液的体积无关,B符合题意;C、溶液中Cl–的数目=nNA=cVNA,所以与溶液的体积有关,C不合题意;D、溶液的密度与溶液的体积无关,D符合题意;答案为BD。(3)①设需要量取的浓盐酸的体积为V,则11.9mol·L–1×V=0.5L×0.400mol·L–1,V=0.0168L=16.8mL,故答案为16.8;②配制溶液时除烧杯和玻璃棒,还需要的仪器有量筒、500mL容量瓶、胶头滴管;③实验开始时,需要检查容量瓶是否漏水;④配制溶液时,操作步骤为:称量→溶解→冷却→转移→洗涤→定容→摇匀,故答案为:FCEGABD;⑤Ⅰ、用量筒量取浓盐酸时俯视观察凹液面,则所取浓盐酸的体积偏小,所配溶液的浓度偏小;Ⅱ、定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水,溶液的体积偏大,所以配制溶液的浓度偏小;Ⅲ、配制时,容量瓶有少量蒸馏水,不会影响溶液体积,也不会影响所配溶液中溶质的物质的量,所以不会影响溶液浓度;Ⅳ、定容时仰视刻度线,则溶液的体积偏大,配得的溶液浓度偏小。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
A.18gNH 含有电子数为10NA 含有电子数为10NA |
| B.1mol任何气体的体积都约是22.4L |
| C.NA个H2SO4分子的质量等于H3PO4的摩尔质量 |
| D.标准状况下,相同体积的O2、HCl、H2O含有的分子数相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.150 mL 1 mol·L-1的KClO3 | B.150 mL 3 mol·L-1的KCl |
| C.75 mL 2 mol·L-1的CaCl2 | D.75 mL 2 mol·L-1的NH4Cl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
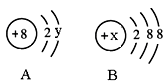
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.0 L 1.0 mo1·L-1的NaAlO2水溶液中含有的氧原子数为2 NA |
| B.12g石墨烯(单层石墨)中含有六元环的个数为0.5 NA |
| C.25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 NA |
| D.1 mol的—OH与1 mol的OH一所含电子数均为9 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10 mL 0.5 mol·L–1 Cu(NO3)2溶液 | B.5 mL 0.8 mol·L–1 Al(NO3)3溶液 |
| C.10 mL 2 mol·L–1 AgNO3溶液 | D.10 mL 1 mol·L–1 Mg(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 应取浓硫酸的体积/ml | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 一定含有的离子种类 | | | | | | | |
| 物质的量浓度(mol/L) | | | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.3g金属钠与过量的氧气反应,无论是否加热与否转移电子数均为0.1NA |
| B.1mol Na2CO3晶体中含CO32-离子数小于NA |
| C.惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体11.2L |
| D.0.1mol的CaO2中含阴离子数是0.2 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com