
| A. | 将SO2通入含HClO的溶液中生成H2SO4,说明HClO的酸性比H2SO4强 | |
| B. | 实验室做钠的实验时,余下的钠屑投入到废液缸中 | |
| C. | SiO2可以和NaOH溶液及HF溶液反应,SiO2属于两性氧化物 | |
| D. | 皮肤上沾有少量浓硝酸时,立刻用大量水冲洗,再涂上稀碳酸氢钠溶液 |
分析 A.二氧化硫被次氯酸氧化成硫酸,只能说明次氯酸具有较强氧化性,无法判断次氯酸与硫酸的酸性大小;
B.金属钠性质活泼,易与空气中的氧气、水等反应;
C.二氧化硅能够与碱溶液反应生成盐和水,二氧化硅属于碱性氧化物,但二氧化硅与氟化氢以外的酸不反应,不属于碱性氧化物;
D.硝酸有强氧化性.
解答 解:A.将SO2通入含HClO的溶液中生成H2SO4,证明次氯酸具有较强氧化性,不能证明次氯酸、硫酸的酸性大小,实际上次氯酸为弱酸,硫酸为强酸,次氯酸的酸性小于硫酸,故A错误;
B.金属钠性质活泼,易与空气中的氧气、水等反应,如投入到废液缸中,易产生火灾,应放回原试剂瓶,故B错误;
C.二氧化硅能够与氢氧化钠溶液反应生成盐和水,二氧化硅属于酸性氧化物,对应的酸为硅酸;而二氧化硅不与氟化氢以外的酸反应,不属于碱性氧化物,即二氧化硅不属于两性氧化物,故C错误;
D.硝酸有强氧化性,应立刻用大量水冲洗,再涂上稀碳酸氢钠溶液,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及氧化还原反应与、二氧化硅的性质、次氯酸的性质以及危险的处理等,题目难度中等,把握化学反应原理及物质性质为解答的关键,注意对常见化学实验方案的评价方法.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:选择题
| A. | 高纯硅可用于制造半导体材料 | |
| B. | 水玻璃可用于生产黏合剂和防火剂 | |
| C. | 玻璃、水泥、陶瓷、石英的成分中均含有硅酸盐 | |
| D. | Si3N4是一种新型无机非金属材料,可用于制造发动机 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中FeSO4既作氧化剂,又作还原剂 | |
| B. | SO2能使溴水褪色,说明SO2具有漂白性 | |
| C. | 该反应中每生成1molFe2O3转移电子数约为1×6.02×1023 | |
| D. | 该反应生成的气体通入足量BaCl2溶液中,可得到BaSO3和BaSO4两种沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
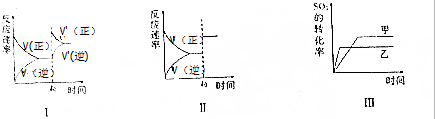
| A. | 图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 | |
| B. | 图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 | |
| C. | 图Ⅲ研究的是压强对化学平衡的影响,且乙的压强比甲高 | |
| D. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度比甲高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、I- | |
| B. | 含Br-、K+、Na+、HSO3-的溶液,通入SO2后这些离子仍能大量共存 | |
| C. | 含K+、Na+、NO3-、CH3COO-的溶液中c(H+)=$\sqrt{{K}_{W}}$ | |
| D. | 在水电离出的c(H+)=10-13mol•L-1 的溶液中:NH4+、AlO2-、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
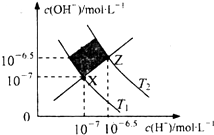
| A. | XZ线上任意点均表示溶液的pH=7 | |
| B. | 图中T1>T2 | |
| C. | M区域对应溶液中大量存在:Fe3+、Na+、C1-、SO42- | |
| D. | Z点对应的可能是CH3COOH和CH3COONa的混合液,且c(CH3COO-)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SiO3. H2S CO2 | B. | H2O NH3•H2O HClO HF | ||
| C. | H2SO3. Ba(OH)2 BaSO4 | D. | H2SO3. Ba(OH)2 BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分解反应 | B. | 复分解反应 | C. | 置换反应 | D. | 化合反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com