
| A. | 酸性氧化物:CO2、SO2、SiO2 | B. | 混合物:漂白粉、氨水、铝热剂 | ||
| C. | 电解质:氯气、硫酸钡、酒精 | D. | 同素异形体:C60、金刚石、石墨 |
分析 A、与碱反应生成盐和水的氧化物为酸性氧化物;
B、由不同物质组成的为混合物,根据物质的组成情况来回答;
C、在水溶液中或熔融状态下能导电的化合物为电解质;
D、同素异形体是同种元素组成的性质不同单质之间的互称.
解答 解:A、CO2、SO2、SiO2都和强碱溶液反应生成盐和水,属于酸性氧化物,故A正确;
B、漂白粉为氯化钙和次氯酸钙的混合物、氨水是一水合氨的溶液、铝热剂混合物时铝和金属氧化物的混合物,故B正确;
C、氯气是单质不是电解质、硫酸钡属于盐为强电解质、酒精是非电解质,故C错误;
D、C60、金刚石、石墨是碳元素组成的性质不同单质,互为同素异形体,故D正确.
故选C.
点评 本题考查了物质分类的方法和依据,掌握基础,概念的理解应用是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
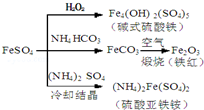
| A. | 碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂 | |
| B. | 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 | |
| C. | 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 | |
| D. | 常温下,(NH4)2Fe(SO4)2比FeSO4易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

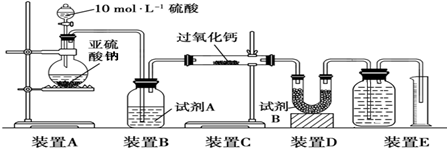
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 铜粉与稀硝酸的反应:Cu+2H+═Cu2++H2↑ | |
| C. | 氢氧化铜与稀盐酸反应:OH-+H+═H2O | |
| D. | 碳酸钠溶液与足量稀硫酸的反应:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
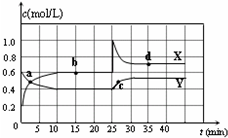 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )| A. | 图中Y曲线是表示NO2浓度随时间的变化曲线 | |
| B. | 前10 min内v(N2O4)为0.1 mol/( L•min) | |
| C. | 25 min时,导致平衡移动的原因是将密闭容器的体积缩小为1L | |
| D. | 25 min时,导致平衡移动的原因是向容器通入适量NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1LCO2中含有3NA个原子 | |
| B. | 1molCl2含有1NA个原子 | |
| C. | 23g钠在足量的Cl2中反应,转移电子数NA个 | |
| D. | 欲配制1.00L1.00mol•L-1的NaCl溶液,可将58.5gNaCl溶于1.00L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com