
【题目】常温常压下,用电火花引爆 H2 和 Cl2 所组成的混合气体,反应停止后再恢复到原来的温度和压强, 测得气体体积与发生反应前恰好相等.则下列叙述合理的是( )
A. 与原混合气体中 H2 和 Cl2 的体积配比无关
B. 原混合气体中 H2 的体积一定大于 Cl2 的体积
C. 原混合气体中 H2 的体积一定小于 Cl2 的体积
D. 原混合气体中 H2 的体积恰好与 Cl2 的体积相等
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质性质的比较,错误的是( )
A.溶解度(25℃):小苏打 < 苏打B.沸点:H2Se>H2S>H2O
C.密度:溴乙烷 > 水D.碳碳键键长:乙烯 < 苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究木炭与浓H2SO4反应的产物中是否存在CO2,某同学选用下图所示装置进行实验:
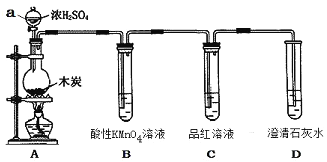
(1)仪器a的名称为:___________;在组装好上述实验装置后,在装入药品之前必需的实验操作是___________。
(2)写出A中发生反应的化学方程式_______________。
(3)装置B的作用是_______;该装置中发生的化学反应可说明SO2具有_______________性。
(4)已知SO2也可以使澄清的石灰水变浑浊,则能说明产物中一定存在CO2气体的实验现象为______________,____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表:
化合物 | 相对分 | 密度 | 沸点/℃ | 溶解度 |
正丁醇 | 74 | 0.80 | 118.0 | 9 |
冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
操作如下:
①在50mL圆底烧瓶中,加入18.5mL正丁醇和13.4mL冰醋酸,3~4滴浓硫酸,投入沸石.安装分水器(作用:实验过程中不断分离除去反应生成的水)及回流冷凝管.
②将分水器分出的酯层和反应液一起倒入分液漏斗中,水洗,10% Na2CO3洗涤,再水洗,最后转移至锥形瓶,干燥.
③将干燥后的乙酸正丁酯滤入烧瓶中,常压蒸馏,收集馏分,得15.1g乙酸正丁酯.
请回答有关问题:
(1)冷水应该从冷凝管(填“a”或“b”)端管口通入.
(2)进行分液操作时,使用的漏斗是(填选项).
(3)仪器A中乙酸和正丁醇制备乙酸正丁酯的化学方程为 .
(4)步骤①“不断分离除去反应生成的水”的目的是 .
(5)步骤②中用10% Na2CO3溶液洗涤有机层,该步操作的目的是
(6)乙酸正丁酯的产率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅笔芯的主要成分是石墨。如果铅笔芯写一个字消耗的石墨质量约为1×10-3g,那么一个铅笔字含有的碳原子数约为
A. 5×1019个B. 5×1022个C. 2.5×1022个D. 2.5×1019个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CO2 通入体积为 50mL 的 NaOH 溶液中,为了测定应后溶液的成分,向其中滴加 1.0mol/L 的盐酸,加入盐酸的体积和生成 CO2的体积(标准状况下)的关系如图所示。

(1)OA 段发生反应的离子方程式为:_______________________________。
(2)溶液中溶质是:_____________,其物质的量之比为______________。
(3)原 NaOH 溶液的物质的量浓度为_____________。
(4)原 NaOH 溶液中通入 CO2 气体体积_________mL。
(5)当向 NaOH 溶液中通入少量 CO2时,溶液中的溶质是 NaOH 和 Na2CO3,设计如下实验证明该溶质的组成,请补充完整。
实验方案 | 实验现象 | 实验结论 |
取少量溶液于试管中,加入足量 BaCl2溶液 | ___________ | 说明溶液中含有 Na2CO3 |
___________ | ___________ | 说明溶液中含有 NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种固态物质熔化(或气化)时,克服的微粒间相互作用力属于同种类型的是( )
A.碘和氯化钾
B.金刚石和重晶石
C.二氧化硅和干冰
D.软脂酸甘油酯和冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①有单质参加或生成的反应一定是氧化还原反应
②向Al2(SO4)3溶液中逐滴滴加Ba(OH)2溶液,先生成白色沉淀,后沉淀消失
③向含有BaCl2和NaOH的混合溶液中通入少量的二氧化硫气体,有白色沉淀生成
④向CaCl2溶液中通入足量二氧化碳气体,先生成白色沉淀,后沉淀消失
⑤101kPa、150℃时,agCO和H2的混合气体在足量的O2中完全燃烧,将燃烧后的产物通入足量的Na2O2固体后,Na2O2增重ag
⑥为测定熔融氢氧化钠的导电性,可在刚玉(主要成分是Al2O3) 坩埚中熔化氢氧化钠固体后进行测量
⑦碱性氧化物一定是金属氧化物
⑧22.4L的CO气体和28gN2所含的电子数相等
A. ①②④⑥⑧ B. ③④⑤ C. ①⑤⑥⑦ D. ③⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是( )
A.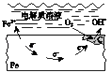
钢铁表面水膜的酸性很弱或呈中性,发生吸氧腐蚀
B.
钢铁表面水膜的酸性较强,发生析氢腐蚀
C.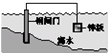
将锌板换成铜板对钢闸门保护效果更好
D.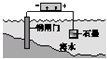
钢闸门作为阴极而受到保护
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com