
(8分)已知四种白色粉末分别是KNO3、MgCl2、Ba(OH)2、无水CuSO4中的一种。现只提供蒸馏水一种试剂,对这些物质进行鉴别(被鉴别出的物质可作为试剂来鉴别其他物质)。请按要求填写下列表格:
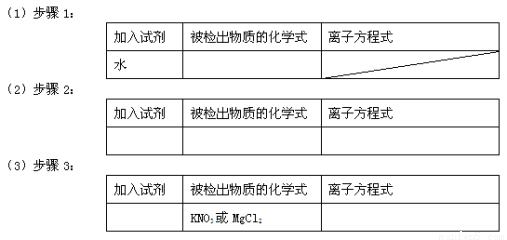
(8分)⑴步骤1:
| CuSO4 (1分) |
|
⑵步骤2:
CuSO4 (1分) | Ba(OH)2 (1分) | Cu2++2OH-+Ba2++SO42-==Cu(OH)2↓+BaSO4↓ (2分) |
⑶步骤3:
Ba(OH)2 (1分) |
| Mg2++2OH-====Mg(OH)2 ↓ (2分) |
【解析】
试题分析:(1)KNO3、MgCl2、Ba(OH)2、无水CuSO4中,加入水后,只有硫酸铜溶液为蓝色,所以加水就鉴别出来的物质是CuSO4;
(2)CuSO4被鉴别出来后就可作为已知试剂,进行鉴别其他物质。硫酸铜只与剩余三种物质中的氢氧化钡反应生成氢氧化铜蓝色沉淀和硫酸钡白色沉淀,所以加入CuSO4,可鉴别出来的物质是Ba(OH)2,反应的离子方程式是Cu2++2OH-+Ba2++SO42-==Cu(OH)2↓+BaSO4↓
(3)氢氧化钡鉴别出来后,再用氢氧化钡作已知试剂,鉴别剩余两种物质,氢氧化钡与氯化镁反应生成白色沉淀,所以加入Ba(OH)2,可鉴别出MgCl2,剩下的就是硝酸钾,反应的离子方程式是Mg2++2OH-====Mg(OH)2 ↓。
考点:考查物质的逐一鉴别法,离子方程式的书写


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、研究高温下活性较大的催化剂 |
| B、研究低温下活性较大的催化剂 |
| C、寻求氨的新来源 |
| D、研制耐高温高压的新型材料建造合成塔 |
查看答案和解析>>
科目:高中化学 来源:2013年普通高等学校招生全国统一考试化学(广东卷解析版) 题型:简答题
(16分)大气中的部分碘源于O3对海水中I-的氧化。将O3持续通入NaI溶液中进行模拟研究。
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+ O3(g)==IO-(aq)+O2(g) △H1
②IO-(aq)+H+(aq)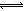 HOI(aq) △H2
HOI(aq) △H2
③HOI(aq)+ I-(aq)+ H+(aq)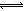 I2(aq)+H2O(l) △H3
I2(aq)+H2O(l) △H3
总反应的化学方程式为______,其反应△H=______。
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)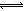 I3-(aq),其平衡常数表达式为_______。
I3-(aq),其平衡常数表达式为_______。
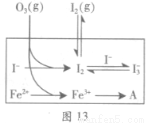
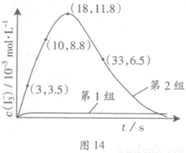
(3)为探究Fe2+对氧化I-反应的影响(反应体系如图13),某研究小组测定两组实验中I3-浓度和体系pH,结果见图14和下表。
编号 | 反应物 | 反应前pH | 反应后pH |
第1组 | O3+ I- | 5.2 | 11.0 |
第2组 | O3+ I-+ Fe2+ | 5.2 | 4.1 |
①第1组实验中,导致反应后pH升高的原因是_______。
②图13中的A为 。由Fe3+生成A的过程能显著提高I-的转化率,原因是_______。
③第2组实验进行18s后,I3-下降。导致下降的直接原因有(双选)______。
A.c(H+)减小 B.c(I-)减小 C.I2(g)不断生成 D.c(Fe3+)增加
(4)据图14,计算3~18s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市房山区下学期高二期末测验化学试卷(解析版) 题型:选择题
下列说法正确的是
A.某温度时, 1LpH=6的水溶液,含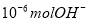 离子
离子
B.含10.6gNa2CO3溶液中,所含阴离子总数等于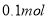
C.VLamol/LFeCl3溶液中,若Fe3+离子数目为1mol,则Cl-离子数目大于3mol。
D.电解精炼粗铜时,每转移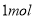 电子,阳极上溶解的
电子,阳极上溶解的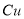 原子数必为
原子数必为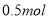
查看答案和解析>>
科目:高中化学 来源:2014秋季江西省赣州市十二县高一上学期期中联考化学试卷(解析版) 题型:选择题
浓H2SO4和木炭在加热时发生反应的化学方程式是:2H2SO4(浓)+C=CO2↑+2H2O+2SO2↑,则12g木炭和足量的浓硫酸反应后生成的气体在标况下的体积为
A.22.4L B.44.8L C.67.2L D.89.6L
查看答案和解析>>
科目:高中化学 来源:2014秋季江西省赣州市十二县高一上学期期中联考化学试卷(解析版) 题型:选择题
菜谱中记载:河虾不能与西红柿同食,主要原因是因为河虾中含有+5价砷(As),西红柿中含有比较多的维生素C,两者同食会产生有毒的+3价砷,下列说法中正确的是
A.中毒过程中+5价砷体现出一定的还原性
B.中毒过程中,维生素C作氧化剂
C.因为河虾中含有砷元素,所以不能食用
D.+3价砷具有还原性
查看答案和解析>>
科目:高中化学 来源:2014秋北京市高一上学期期中化学试卷(解析版) 题型:填空题
(6分)铁丝在氯气中点燃发生反应:2Fe + 3Cl2  2FeCl3,其中氯元素的化合价_______(填“升高”或“降低”),氯元素被____ _____(填“氧化”或“还原”);Fe做_____ ____剂,具有 性。在该反应中,若消耗了1 mol Fe,则生成___ ____mol FeCl3,转移 mol电子。
2FeCl3,其中氯元素的化合价_______(填“升高”或“降低”),氯元素被____ _____(填“氧化”或“还原”);Fe做_____ ____剂,具有 性。在该反应中,若消耗了1 mol Fe,则生成___ ____mol FeCl3,转移 mol电子。
查看答案和解析>>
科目:高中化学 来源:2014秋北京市高一上学期期中化学试卷(解析版) 题型:选择题
丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1 g/mL,沸点约55 oC,分离水和丙酮时最合理的方法是
A.蒸发 B.分液 C.过滤 D.蒸馏
查看答案和解析>>
科目:高中化学 来源:2014秋北京市高一上学期期中化学试卷(解析版) 题型:选择题
下列各组混合物不能用分液漏斗分离的是
A.四氯化碳和碘 B.花生油和水
C.四氯化碳和水 D.水和汽油
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com