
| A. | NH4Cl的电子式: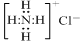 | |
| B. | 2-硝基甲苯的结构简式: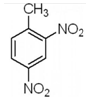 | |
| C. | 硫原子结构示意图: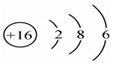 | |
| D. | 质子数为94、中子数为144的钚原子:${\;}_{94}^{144}$Pu |
分析 A、氯化铵是由氨根离子与氯离子通过离子键结合而成的离子化合物;
B、2-硝基甲苯是在甲苯苯环上的2号碳原子上连有一个硝基;
C、硫原子的核内有16个质子,核外有16个电子;
D、质量数=质子数+中子数.
解答 解:A、氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: ,故A错误;
,故A错误;
B、2-硝基甲苯是在甲苯苯环上的2号碳原子上连有一个硝基,故结构简式为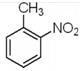 ,故B错误;
,故B错误;
C、硫原子的核内有16个质子,核外有16个电子,故原子结构示意图为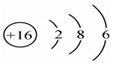 ,故C正确;
,故C正确;
D、质量数=质子数+中子数,故质子数为94、中子数为144的钚原子的质量数为238,即为23894Pu,故D错误.
故选C.
点评 本题考查了常见额化学用语,难度不大,应注意的是离子化合物电子式的书写方法.


科目:高中化学 来源: 题型:解答题
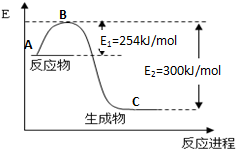 到目前为止,由化学能转变的热能或电能仍然是人类使用最广泛的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用最广泛的能源.| 化学键 | H-H | N≡N |
| 键能(kJ/mol) | 435 | 943 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃 | |
| B. | 分子组成符合CnH2n+2的烃一定是烷烃 | |
| C. | 正戊烷分子中所有原子均在一条直线上 | |
| D. | CH3CH(CH3)2在光照下与氯气反应,可以生成四种一氯代烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| B. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| C. | 若在原电池中进行,反应放出的热量不变 | |
| D. | 升高温度,反应速率加快,反应放出的热量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,2-二甲基-1-丁醇与2-甲基-2-丁醇互为同分异构体 | |
| B. |  的核磁共振氢谱有5个峰 的核磁共振氢谱有5个峰 | |
| C. | 根据核磁共振氢谱能鉴别1-溴丙烷和2-溴丙烷 | |
| D. | 用KMnO4酸性溶液能鉴别CH3CH═CHCH2OH和CH3CH2CH2CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 虽然药物能治病,但大部份药物有毒副作用 | |
| B. | 青霉素有解热镇痛的作用 | |
| C. | 阿司匹林是最重要的抗生素 | |
| D. | 随着药物的普及,生病了都可以到药店自己买药吃,不用到医院 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4mol | B. | 2mol | C. | 1mol | D. | 3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com