
【题目】(1)标准生成热指的是在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下 1mol 某纯物质的热效应,单位常用 kJ/mol表示,已知在 25℃的条件下:
①Ag2O(s)+2HCl(g)═2AgCl(s)+H2O(l)△H=-324.4 kJ/mol
②2Ag(s)+ ![]() O2(g)═Ag2O(s)△H=-30.56kJ/mol
O2(g)═Ag2O(s)△H=-30.56kJ/mol
③ ![]() H2(g)+
H2(g)+ ![]() Cl2(g)═HCl(g)△H=-92.21 kJ/mol
Cl2(g)═HCl(g)△H=-92.21 kJ/mol
④H2(g)+ ![]() O2(g)═H2O(l)△H=-285.6 kJ/mol
O2(g)═H2O(l)△H=-285.6 kJ/mol
则25℃时氯化银的标准生成热为________ kJ/mol;
(2)实验测得 64g 甲醇[CH3OH(l)]在氧气中充分燃烧生成 CO2 气体和液态水时放出 1452.8kJ 的热量,则表示甲醇燃烧热的热化学方程式_________________;
(3)以甲烷、氧气为原料,KOH 为电解质,构成燃料电池,写出其负极的电极反应式:________;
(4)电解法制取有广泛用途的 Na2FeO4,工作原理如下图所示。
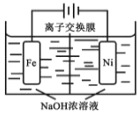
已知:Na2FeO4 只在强碱性条件下稳定。
①Na2FeO4能够净水的主要原因是_______________ 。
②阳极电极反应式 _______________;
③为使电解能较持久进行,应选用_______________ 离子交换膜(填“阴”或“阳”)。
【答案】-126.89 CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l)△H=-726.4kJ/mol CH4+2O2+2OH-=CO32-+3H2O Na2FeO4具有强氧化性,能够杀菌消毒,在杀菌消毒的过程中被还原为+3价的铁,水解生成具有强吸附性的氢氧化铁胶体,能够吸附水中杂质 Fe-6e-+8OH-═FeO42-+4H2O 阴
O2(g)=CO2(g)+2H2O(l)△H=-726.4kJ/mol CH4+2O2+2OH-=CO32-+3H2O Na2FeO4具有强氧化性,能够杀菌消毒,在杀菌消毒的过程中被还原为+3价的铁,水解生成具有强吸附性的氢氧化铁胶体,能够吸附水中杂质 Fe-6e-+8OH-═FeO42-+4H2O 阴
【解析】
(1)依据标准生成热指的是在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下1mol某纯物质的热效应,结合热化学方程式和盖斯定律计算分析得到;
(2)依据题干条件计算1mo甲醇燃烧放出的热量,依据热化学方程式的书写方法写出甲醇燃烧热的热化学方程式;
(3)原电池中负极上燃料失电子,碱性条件下,CH4反应生成碳酸根离子;
(4)①Na2FeO4中的铁元素为+6价,具有强氧化性,在杀菌消毒的过程中被还原为+3价的铁,能够水解生成氢氧化铁胶体,据此分析解答;②金属铁是阳极,该电极上金属铁发生失电子的氧化反应,在碱性条件下生成FeO42-;③Na2FeO4只在强碱性条件下稳定,电解过程中OH-向阳极移动,据此分析判断。
(1)①Ag2O(s)+2HCl(g)═2AgCl(s)+H2O(l)△H=-324.4 kJ/mol,②2Ag(s)+ ![]() O2(g)═Ag2O(s) △H=-30.56kJ/mol,③
O2(g)═Ag2O(s) △H=-30.56kJ/mol,③ ![]() H2(g)+
H2(g)+ ![]() Cl2(g)═HCl(g) △H=-92.21 kJ/mol,④H2(g)+
Cl2(g)═HCl(g) △H=-92.21 kJ/mol,④H2(g)+ ![]() O2(g)═H2O(l) △H=-285.6 kJ/mol,根据盖斯定律:将①+②+③×2-④得到:2Ag(s)+Cl2(s)=2AgCl(s) △H=-253.78kJ/mol,所以氯化银的标准生成热为
O2(g)═H2O(l) △H=-285.6 kJ/mol,根据盖斯定律:将①+②+③×2-④得到:2Ag(s)+Cl2(s)=2AgCl(s) △H=-253.78kJ/mol,所以氯化银的标准生成热为 ![]() ×(-253.78kJ/mol)=-126.89 kJ/mol,故答案为:-126.89;
×(-253.78kJ/mol)=-126.89 kJ/mol,故答案为:-126.89;
(2)64g液态甲醇在氧气中充分燃烧生成二氧化碳和液态水时,放出1452.8kJ的热量,则32g液态甲醇燃烧生成二氧化碳和液态水放热 ![]() ×1452.8kJ=726.4kJ,反应的热化学方程式为:CH3OH(l)+
×1452.8kJ=726.4kJ,反应的热化学方程式为:CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l) △H=-726.4kJ/mol,故答案为:CH3OH(l)+
O2(g)=CO2(g)+2H2O(l) △H=-726.4kJ/mol,故答案为:CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) △H=-726.4kJ/mol;
O2(g)=CO2(g)+2H2O(l) △H=-726.4kJ/mol;
(3)原电池放电时,负极上甲烷失电子被氧化,电极反应式为:CH4+2O2+2OH-=CO32-+3H2O,故答案为:CH4+2O2+2OH-=CO32-+3H2O;
(4)①Na2FeO4中的铁元素为+6价,具有强氧化性,能够杀菌消毒,在杀菌消毒的过程中被还原为+3价的铁,水解生成具有强吸附性的氢氧化铁胶体,能够吸附水中的细微悬浮物形成沉淀,所以是一种“绿色、环保、高效”净水剂,故答案为:Na2FeO4具有强氧化性,能够杀菌消毒,在杀菌消毒的过程中被还原为+3价的铁,水解生成具有强吸附性的氢氧化铁胶体,能够吸附水中杂质;
②根据图示,金属铁是阳极,该电极上金属铁发生失电子的氧化反应,即Fe-6e-+8OH-═FeO42-+4H2O,故答案为:Fe-6e-+8OH-═FeO42-+4H2O;
③Na2FeO4只在强碱性条件下稳定,电解过程中OH-向阳极移动,则应选择阴离子交换膜,故答案为:阴。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】绿色植物标本用醋酸铜[(CH3COO)2Cu]处理后颜色更鲜艳、稳定。某化学小组制备醋酸铜晶体并测定产品中铜的含量,实验如下。
Ⅰ.醋酸铜晶体的制备

(1)①中,用离子方程式表示产物里OH-的来源是__________。
(2)②中,化学方程式是__________。
(3)③中采用的实验方法依据醋酸铜的性质是_________。
Ⅱ.测定产品中铜的含量
ⅰ.取a g醋酸铜产品于具塞锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产生CuI沉淀,溶液呈棕黄色;
ⅱ.用b molL-1 Na2S2O3标准溶液滴定ⅰ中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;
ⅲ.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
ⅳ.继续用Na2S2O3 标准溶液滴定ⅲ中浊液至终点,消耗标准溶液v mL。
已知:①![]() ,Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
,Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②CuI易吸附I2,CuSCN难溶于水且不吸附I2。被吸附的I2不与淀粉显色。
(4)ⅰ中发生反应的离子方程式是__________。
(5)结合离子方程式说明,ⅲ中加入KSCN的目的是__________。
(6)醋酸铜产品中铜元素的质量分数是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己酮(![]() )在生产生活中有重要的用途,可在酸性溶液中用环己醇间接电解氧化法制备,其原理如图所示。下列说法正确的是
)在生产生活中有重要的用途,可在酸性溶液中用环己醇间接电解氧化法制备,其原理如图所示。下列说法正确的是
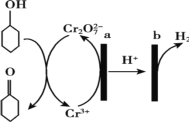
A.a 极与电源负极相连
B.a 极电极反应式是 2Cr3+- 6e- +14OH-= Cr2O72-+7H2O
C.b 极发生氧化反应
D.理论上生成 1mol 环己酮时,有 1molH2 生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A.36g冰中含有氢键的数目为2NA
B.100g30%的甲醛水溶液中所含的氧原子数目为1NA
C.1molCl2与足量铁粉完全燃烧,转移的电子数为3NA
D.14gFe发生电化学腐蚀最终生成Fe2O3·xH2O,电极反应转移的电子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 A 与 H2、CO 以物质的量 1∶1∶1 的比例形成 B,B能发生银镜反应,C 分子中只有一种氢,相关物质转化关系如下(含有相同官能团的有机物通常具有相似的化学性质):

请回答:
(1)有机物 C 的结构简式是________,反应②的反应类型是________。
(2)写出一定条件下发生反应①的化学方程式___________。
(3)下列说法不正确的是________(填字母)。
A.化合物 A 属于烃
B.化合物 D 含有两种官能团
C.用金属钠无法鉴别化合物 F、G
D.A 与 D 一定条件下可以生成 CH3CH2OCH2CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知侯氏制碱法的主要反应为NaCl + NH3 + CO2 + H2O = NaHCO3↓ + NH4Cl。某实验小组模拟工业生产制备少量NaHCO3,将实验流程分为制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤。下列图示装置和操作能达到实验目的的是
A. 制取氨气B.
制取氨气B. 制取NaHCO3
制取NaHCO3
C.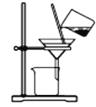 分离NaHCO3D.
分离NaHCO3D.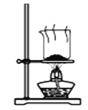 干燥NaHCO3
干燥NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
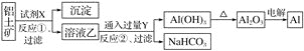
下列叙述不正确的是( )
A.试剂X可以是氢氧化钠溶液
B.反应①过滤后所得沉淀为氧化铁
C.图中所示转化反应包含氧化还原反应
D.反应②的化学方程式为2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应与能量变化的说法正确的是
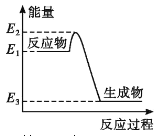
A. 如图所示的化学反应中,反应物的键能之和大于生成物的键能之和
B. 相同条件下,氢气和氧气反应生成液态水比生成等量的气态水放出的热量少
C. 金刚石在一定条件下转化成石墨能量变化如图所示,热反应方程式可为:C(s金刚石) =C(s,石墨) H=-(E2—E3)kJ·mol—1
D. 同温同压下,H2(g)+C12(g)==2HCl(g)能量变化如图所示,在光照和点燃条件下的△H相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某气体的摩尔质量为M g·mol-1,分子数目为N,质量是m g,阿伏加德罗常数为NA,m(C)为12C原子质量,试说明下列各式所表示的意义。
①![]() ________________________________。
________________________________。
②![]() _______________________________。
_______________________________。
③![]() ___________________________________。
___________________________________。
④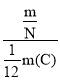 _____________________。
_____________________。
(2)下列气体在同温度、同体积、同质量时,压强最大的是(_______________)
A.CO2 B.CO C.CH4 D.H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com