
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A.SO3与SO2
B.BF3与NH3
C.BeCl2与SCl2
D.H2O与SO2
【答案】A
【解析】解:A、SO3中S原子杂化轨道数为 ![]() (6+0)=3,采取 sp2杂化方式,SO2中S原子杂化轨道数为
(6+0)=3,采取 sp2杂化方式,SO2中S原子杂化轨道数为 ![]() (6+0)=3,采取 sp2杂化方式,故A正确. B、BF3中B原子杂化轨道数为
(6+0)=3,采取 sp2杂化方式,故A正确. B、BF3中B原子杂化轨道数为 ![]() (3+3)=3,采取 sp2杂化方式,NH3中N原子杂化轨道数为
(3+3)=3,采取 sp2杂化方式,NH3中N原子杂化轨道数为 ![]() (5+3)=4,采取 sp3杂化方式,二者杂化方式不同,故B错误;
(5+3)=4,采取 sp3杂化方式,二者杂化方式不同,故B错误;
C、BeCl2中Be原子杂化轨道数为 ![]() (2+2)=2,采取 sp杂化方式,SCl2中S原子杂化轨道数为
(2+2)=2,采取 sp杂化方式,SCl2中S原子杂化轨道数为 ![]() (6+2)=4,采取 sp3杂化方式,二者杂化方式不同,故C错误;
(6+2)=4,采取 sp3杂化方式,二者杂化方式不同,故C错误;
D、H2O中O原子杂化轨道数为 ![]() (6+2)=4,采取sp3杂化方式,SO2中S原子杂化轨道数为
(6+2)=4,采取sp3杂化方式,SO2中S原子杂化轨道数为 ![]() (6+0)=3,采取sp2杂化方式,中心原子杂化轨道的类型不同,故D错误.
(6+0)=3,采取sp2杂化方式,中心原子杂化轨道的类型不同,故D错误.
故选:A.
A、B、C、D物质属于ABm,ABm型杂化类型的判断:
公式:电子对数n= ![]() (中心原子的价电子数+配位原子的成键电子数±电荷数)
(中心原子的价电子数+配位原子的成键电子数±电荷数)
注意:①当上述公式中电荷数为正值时取“﹣”,电荷数为负值时取“+”.②当配位原子为氧原子或硫原子时,成键电子数为零.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为: 2KClO3 +4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况:(单线桥法表示)________________________。
(2)氧化剂与还原剂的物质的量之比是 ___________________
(3)若产生标况下22.4 L Cl2,则转移的电子的物质的量为________mol。
(4)实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸中HCl的物质的量浓度 mol·L-1。
(5)ClO2对污水中Fe2+、Mn2+、S2-和CN- 等有明显的去除效果。某工厂污水中含CN- a mg/L,现用ClO2将CN - 氧化,只生成两种气体,其离子反应方程式为为 ,处理100 m3这种污水,至少需要ClO2 _______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京提出2008年“绿色奥运”的口号,为改善北京空气质量,将冬季燃烧煤取暖改用天然气做燃料.主要是为了( )
A.减少氮氧化物的排放
B.降低对臭氧层的破坏
C.减少二氧化碳的排放
D.防止温室效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合所学内容,完成下列问题:
(1)过氧化钠固体的颜色是______________。
(2)写出磁性氧化铁的化学式_____________,小苏打的化学式____________。
(3)写出实验室加热NH4Cl和Ca(OH)2的混合物制取NH3的化学方程式:_______。
(4)若要提取饱和碘水中的碘,所用的萃取剂可以是___________(填序号)。
① 四氯化碳 ② 酒精 ③ 淀粉溶液
(5)红热的木炭与浓硝酸反应的化学方程式为:C+4HNO3(浓)=CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为_________;如果产生标准状况下22.4 L CO2,则转移的电子的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把aL含(NH4)2SO4和NH4NO3的混和溶液分成两等份,一份加入b mol的烧碱并加热,恰好将全部NH4+转变成NH3放出;另一份需含c mol 的BaCl2溶液恰能完全沉淀SO42-,则原溶液中NO3-的物质的的浓度是( )
A. (2b-4c)/a mol/L B. (b-2c)/a mol/L
C. (2b-c)/amol/L D. (b-4c)/a mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法,不正确的是( ) 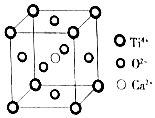
( Ti4+位于顶点上,O2﹣位于面心上,Ca2+位于中心)
A.该晶体的化学式为CaTiO3
B.该晶体中每个Ti4+和8个O2﹣相紧邻
C.一个CO2晶胞中平均含有4个CO2分子
D.金属晶体的熔点可能比分子晶体的熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,前者属于电解质,后者属于非电解质的是( )
A. NaCl晶体、BaSO4 B. 铝、二氧化硫
C. 液态的醋酸、酒精 D. 熔融的KNO3、硫酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究CH3COOH、HA和MOH的酸碱性的相对强弱,某兴趣小组设计了以下实验:室温下,将pH=2的两种酸溶液CH3COOH、HA和pH=12的碱MOH溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图1所示,根据所给数据,请回答下列问题: 
(1)HA为酸 (填“强”或“弱”).稀释后 HA溶液中水电离出来的 c(H+)醋酸溶液中水电离出来c(H+)(填“大于”、“等于”或“小于”).
若b+c=14,则MOH为碱(填“强”或“弱”).
(2)常温下0.10mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变大的是 .
A.c(H+)
B.c(H+)/c(CH3COOH)
C.c(H+)c(OH﹣)
D.c(OH﹣)/(H+)
(3)常温下,用0.10molL﹣1 NaOH溶液分别滴定20mL 0.10molL﹣1 HCl溶液和20mL 0.10 molL﹣1 CH3COOH溶液,得到两条滴定曲线,如图所示.如图中滴定醋酸溶液的曲线是(填“图2”或“图3”);曲线上E点pH>8的原因是(用离子方程式表示) .
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中离子浓度由大到小顺序为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com