
 H++A2£ Ķź³ÉŅŌĻĀĪŹĢā£ŗ
H++A2£ Ķź³ÉŅŌĻĀĪŹĢā£ŗ CaCO3(1)+ SO42-£¬ŅŃÖŖ298KŹ±£¬Ksp[CaCO3]=2.80”Į10-9£¬Ksp[CaSO4]=4.90”Į10-5£¬Ēó“ĖĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżK= (¼ĘĖć½į¹ū±£ĮōČżĪ»ÓŠŠ§Źż×Ö)
CaCO3(1)+ SO42-£¬ŅŃÖŖ298KŹ±£¬Ksp[CaCO3]=2.80”Į10-9£¬Ksp[CaSO4]=4.90”Į10-5£¬Ēó“ĖĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżK= (¼ĘĖć½į¹ū±£ĮōČżĪ»ÓŠŠ§Źż×Ö) HA£+OH£ (2) £¼ (3)1.75”Į10£4
HA£+OH£ (2) £¼ (3)1.75”Į10£4 H++A2£ £¬ÓÉ“ĖæÉŅŌÖŖµĄøĆøĆĖįµÄµŚŅ»²½µēĄėĶźČ«£¬¶ųµŚ¶ž²½µēĄė²»ĶźČ«£¬ĪŖČõĖį£¬¹Ź(1)Na2AČÜŅŗĻŌ¼īŠŌ£¬ĄķÓÉŹĒAĄė×ÓµÄĖ®½ā£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ£ŗB2£+H2O
H++A2£ £¬ÓÉ“ĖæÉŅŌÖŖµĄøĆøĆĖįµÄµŚŅ»²½µēĄėĶźČ«£¬¶ųµŚ¶ž²½µēĄė²»ĶźČ«£¬ĪŖČõĖį£¬¹Ź(1)Na2AČÜŅŗĻŌ¼īŠŌ£¬ĄķÓÉŹĒAĄė×ÓµÄĖ®½ā£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ£ŗB2£+H2O  HA£+OH££»(2)ŅŃÖŖ0.1 mol”¤L£1µÄNaHAČÜŅŗpH=2,¼“ÓÉ HA£µēĄėµÄĒāĄė×ÓÅضČĪŖ0.01mol/L£¬¹ŹH2AČÜŅŗÖŠĒāĄė×ÓµÄĪļÖŹµÄĮæÅضČÓÉÓŚµŚŅ»²½µÄŅÖÖʶųŠ”ÓŚ0.11 mol”¤L-1£»(3)CaSO4(1)+ CO32-
HA£+OH££»(2)ŅŃÖŖ0.1 mol”¤L£1µÄNaHAČÜŅŗpH=2,¼“ÓÉ HA£µēĄėµÄĒāĄė×ÓÅضČĪŖ0.01mol/L£¬¹ŹH2AČÜŅŗÖŠĒāĄė×ÓµÄĪļÖŹµÄĮæÅضČÓÉÓŚµŚŅ»²½µÄŅÖÖʶųŠ”ÓŚ0.11 mol”¤L-1£»(3)CaSO4(1)+ CO32- CaCO3(1)+ SO42-µÄĘ½ŗā³£Źż
CaCO3(1)+ SO42-µÄĘ½ŗā³£Źż H++A2£ £¬ÓÉ“ĖæÉŅŌÖŖµĄøĆøĆĖįµÄµŚŅ»²½µēĄėĶźČ«£¬¶ųµŚ¶ž²½µēĄė²»ĶźČ«£¬±¾ĢāÄѶČÖŠµČ”£
H++A2£ £¬ÓÉ“ĖæÉŅŌÖŖµĄøĆøĆĖįµÄµŚŅ»²½µēĄėĶźČ«£¬¶ųµŚ¶ž²½µēĄė²»ĶźČ«£¬±¾ĢāÄѶČÖŠµČ”£


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā

| | Fe3+ | Al3+ | Mg2+ |
| æŖŹ¼³Įµķ | 2£®1 | 3£®7 | 9£®0 |
| ³ĮµķĶźČ« | 3£®2 | 5£®2 | 12£®4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®KspÖ»ÓėÄŃČܵē½āÖŹµÄŠŌÖŹŗĶĪĀ¶ČÓŠ¹Ų |
| B£®ÓÉÓŚKsp(ZnS)£¾Ksp(CuS)£¬ĖłŅŌZnS³ĮµķŌŚŅ»¶ØĢõ¼žĻĀæÉ×Ŗ»ÆĪŖCuS³Įµķ |
| C£®ĘäĖūĢõ¼ž²»±ä£¬Ąė×ÓÅضČøı䏱£¬Ksp²»±ä |
| D£®Į½ÖÖÄŃČܵē½āÖŹ×÷±Č½ĻŹ±£¬KspŠ”µÄ£¬Čܽā¶ČŅ»¶ØŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®25”ꏱ£¬Fe£ØOH£©3µÄČܽā¶Č“óÓŚAl£ØOH£©3µÄČܽā¶Č |
| B£®25”ꏱ£¬Fe£ØOH£©3µÄČܶȻż“óÓŚAl£ØOH£©3µÄČܶȻż |
| C£®µ±Éś³ÉµÄAl£ØOH£©3Ē”ŗĆĶźČ«ČܽāŹ±£¬ČÜŅŗÖŠµÄČÜÖŹÖ»ÓŠNaAlO2 |
| D£®Ķ¼ÖŠ2a£½b£½6£Øc£b£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 M2+(aq)+2OH-(aq) Ksp=a£¬c(M2+)="b" mol”¤L-1Ź±£¬ČÜŅŗµÄpHµČÓŚ£Ø £©
M2+(aq)+2OH-(aq) Ksp=a£¬c(M2+)="b" mol”¤L-1Ź±£¬ČÜŅŗµÄpHµČÓŚ£Ø £©A£®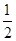 lg( lg(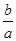 ) ) | B£®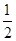 lg( lg(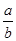 ) ) |
C£®14+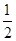 lg( lg(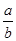 ) ) | D£®14+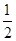 lg( lg(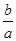 ) ) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÓÉÓŚKsp(Ag2S)<Ksp(AgI)£¬Ļņŗ¬ÅØ¶Č·Ö±šĪŖ0.01mol/LµÄS2£ÓėI£µÄ»ģŗĻČÜŅŗÖŠ¼ÓČė×ćĮæµÄAgNO3(s)£¬Ö»ÓŠAg2S³ĮµķÉś³É |
| B£®FeSŌŚĖ®ÖŠµÄČܽā¶Č“óÓŚŌŚNa2SČÜŅŗÖŠµÄ |
| C£®Ļņŗ¬ÓŠAgCl(s)µÄ±„ŗĶAgClČÜŅŗÖŠ¼ÓĖ®£¬¹ĢĢåAgClÖŹĮæ»į¼õÉŁ£¬µ«AgClµÄČܽā¶ČÓėKsp¾ł²»±ä |
| D£®“ļµ½³ĮµķČܽāĘ½ŗāŹ±£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č²»Ņ»¶ØĻąµČµ«»į±£³Ö²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ČżÖÖ±„ŗĶČÜŅŗÖŠČÜÖŹµÄĪļÖŹµÄĮæÅØ¶ČµÄ“óŠ”Ė³ŠņĪŖc(AgX)£¾c(AgY)£¾c(AgZ) |
| B£®ČōĻņAgYµÄ±„ŗĶČÜŅŗÖŠ¼ÓČėÉŁĮæµÄAgX¹ĢĢ壬Ōņc(Y£)¼õÉŁ |
| C£®ČōČ”0.188gµÄAgY(Ļą¶Ō·Ö×ÓÖŹĮæ188)¹ĢĢå·ÅČė100 mLĖ®ÖŠ(ŗöĀŌČÜŅŗĢå»żµÄ±ä»Æ)£¬ŌņČÜŅŗÖŠY£µÄĪļÖŹµÄĮæÅضČĪŖ1.0”Į10£2mol”¤L£1 |
| D£®ĶłCŃ”ĻīµÄČÜŅŗÖŠ¼ÓČė1 mL 0.1mol”¤L£1µÄNaZČÜŅŗ£¬ÄÜÉś³ÉAgZ³Įµķ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®°±Ė® | B£®ĻõĖį”” | C£®Ė®”” | D£®AgNO3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com