
分析 (1)Cu+具有还原性,NO2-具有氧化性,二者可发生氧化还原反应生成NO,NO2-是氧化剂,表现氧化性;
(2)红棕色气体是NO2,故有NO→N2O+NO2,配平后得:3NO=N2O+NO2,同温同体积时,气体压强比等于其物质的量之比,由此分析解答;
(3)在水中NO与O2反应为4NO+3O2+2H2O=4HNO3,进行计算.
解答 解:(1)Cu+具有还原性,NO2-具有氧化性,二者可发生氧化还原反应生成NO,反应的离子方程式为Cu++NO2-+2H+=Cu2++NO↑+H2O,NO2-是氧化剂,表现氧化性,
故答案为:Cu++NO2-+2H+=Cu2++NO↑+H2O,氧化;
(2)红棕色气体是NO2,故有NO→N2O+NO2,配平后得:3NO=N2O+NO2,同温同体积时,气体压强比等于其物质的量之比,故反应后与反应前容器中压强比为2:3,故答案为:3NO=N2O+NO2,2:3.
(3)在水中NO与O2反应为4NO+3O2+2H2O=4HNO3,0.05molNO和0.03molO2反应氧气不足,由此可求出生成的HNO3的物质的量为0.04mol,故所得硝酸浓度为0.4mol•L-1,故答案为:0.4mol•L-1.
点评 本题考查氮的氧化物的性质及其对环境的影响,化学方程式的书写和相关计算,题目难度不大,注意把握相关基础知识.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | C2H2 | B. | C2H4 | C. | C3H4 | D. | C4H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滤液中一定有Zn(NO3)2 | B. | 滤渣中一定有Cu | ||
| C. | 滤液中一定没有AgNO3 | D. | 滤渣中一定有Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③⑥ | C. | ①③⑤ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有AgBr沉淀生成 | B. | AgCl和AgBr沉淀等量生成 | ||
| C. | AgCl沉淀多于AgBr沉淀 | D. | AgCl沉淀少于AgBr沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福岛核电站泄露的放射性物质131I与127I互为同位素,化学性质几乎相同 | |
| B. | 电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述 | |
| C. | 除去SO2中混有的少量HCl,使气体通过盛有饱和NaHSO3溶液的洗气瓶 | |
| D. | 为了证明氢氧化钠是离子化合物,可在瓷坩埚中将氢氧化钠固体熔化后测其导电性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
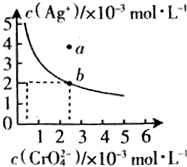 水中的沉淀溶解平衡曲线如图所示. 该温度下.下列说法正确的是AD.
水中的沉淀溶解平衡曲线如图所示. 该温度下.下列说法正确的是AD.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com