
����Ŀ��X��Y��Z��������Ԫ�صĵ����ڳ����¶��dz�������ɫ���壬���ʵ������£�����֮���������������Ӧ���ɷֱ���˫�ˡ����˺��ĺ˵ļס��ҡ������ַ��ӣ����ҡ��������к���XԪ�ص�ԭ�Ӹ�����Ϊ2��3��
��ش��������⣺
(1)Ԫ��X��������_______��
(2)������Y�����ڳ����»�Ͼ�������������Ļ�ѧʽΪ________��
(3)�����ﶡ��X��Y��Z����Ԫ�أ�����һ�ֳ�����ǿ�ᣬ������������ʵ���֮��1��1��Ϻ������������к��еĻ�ѧ��Ϊ________��ѡ����ţ���
a��ֻ�����ۼ� b��ֻ�����Ӽ� c���Ⱥ����Ӽ����ֺ����ۼ�
���𰸡��� 4NH3+5O2![]() 4NO+6H2O c
4NO+6H2O c
��������
X��Y��Z��������Ԫ�صĵ����ڳ����¶��dz�������ɫ���壬�������嵥��Ϊ�������������������������������˫�ˡ����ˡ��ĺ˵ļס��ҡ������ַ��ӣ���ס��ҡ����ֱ�ΪNO��H2O��NH3�����ҡ��������к���XԪ�ص�ԭ�Ӹ�����Ϊ2��3����XΪH������Y�����ڳ����»�Ͼ�������������YΪO����ZΪN�������ﶡ��X��Y��Z����Ԫ�أ���ΪHNO3����������ʵ���֮��1��1��Ϻ�����������ΪNH4NO3�������мȺ����Ӽ����ֺ����ۼ�����NH4+ˮ�������ԣ��ݴ˷������
(1)������������Ԫ��X����������Ԫ�أ�
(2)������������֪����ΪNO����ΪNH3������һ��������ת��Ϊ���ҵķ�Ӧ����ʽΪ4NH3+5O2![]() 4NO+6H2O��
4NO+6H2O��
(3)�����ﶡ��X��Y��Z����Ԫ�أ�����һ�ֳ�����ǿ�ᣬ��ΪHNO3����ΪNH3��������������ʵ���֮��1:1��Ϻ�����������ΪNH4NO3��NH4NO3�����мȺ����Ӽ����ֺ����ۼ�����ѡc��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ����Ҫ�Ĵ�����ϣ������������
����Ҫ�Ĵ�����ϣ������������ ![]() �����Ĺ���ԭ�����£�
�����Ĺ���ԭ�����£�
��2LiAlH4![]() 2LiH��2Al��3H2��
2LiH��2Al��3H2��
��![]()
����˵����ȷ���ǣ� ��
A.![]() �ǹ��ۻ����LiH �����ӻ�����
�ǹ��ۻ����LiH �����ӻ�����
B.����Ӧ��������![]() ��������һ����
��������һ����![]() ������
������
C.���ɵ���������������Ӧ�١���ת�Ƶ�����֮��Ϊ4��3
D.���Ӱ뾶��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij��Br-��ˮ����ȡBr2�Ĺ��̰��������ˡ���������ȡ����ѡ�������ȡ����������Ȳ��衣
��֪����2NaOH+Cl2==NaCl+NaClO+H2O
��Br2�����������Ȼ�̼����ʮ����
���� | Br2 | CCl4 | ��ʮ���� |
�ܶ�/g��cm-3 | 3.119 | 1.595 | 0.753 |
�е㣯�� | 58.76 | 76.8 | 215��217 |
��ˮ���ܽ��� | �� | ���� | ���� |
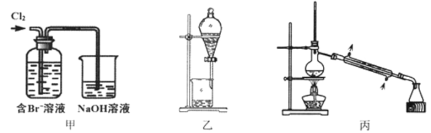
����˵������ȷ����
A. ��װ����Br-�����ķ�ӦΪ��2Br-+Cl2===Br2+2Cl-
B. ��װ����NaOH��Һÿ����1��Cl2��ת��1��e-
C. ����װ�ý�����ȡ���ܽ�Br2���л������²�
D. �ñ�װ�ý����������ռ�������Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������NaNO2����һ�ֳ�����ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������ij��ȤС������ͼ��ʾװ���Ʊ�NaNO2����������������̽����A�м���װ������ȥ����
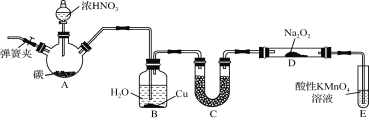
�������زġ�
��2NO��Na2O2=2NaNO2��
��NO�ܱ�����KMnO4������NO![]() ��MnO
��MnO![]() ����ԭΪMn2����
����ԭΪMn2����
��������������NaNO2�ܰ�I������ΪI2��S2O32-�ܰ�I2��ԭΪI����
���Ʊ�NaNO2��
��1�� װ��A������ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2�� Bװ�õ�Ŀ������ ���� ��
��3�� Ϊ��֤�Ƶõ��������ƵĴ��ȣ�Cװ����ʢ�ŵ��Լ������� �����������
A. P2O5 B. ��ʯ�� C. ��ˮCaCl2 D. ��ʯ��
��4�� Eװ�÷�����Ӧ�����ӷ���ʽ�� ��
���ⶨNaNO2���ȡ�
��5�� ��С��ɹ�ѡ����Լ��У�
A.ϡ����
B.c1mol��L-1KI��Һ
C.������Һ
D.c2mol��L-1Na2S2O3��Һ
E.c3mol��L-1����KMnO4��Һ
������NaNO2�Ļ�ԭ�����ⶨ�䴿�ȣ���ѡ����Լ��� �����������
������NaNO2�����������ⶨ�䴿�ȵIJ����ǣ�ȷ��ȡ����Ϊm g��NaNO2��Ʒ������ƿ�У�������ˮ�ܽ� ���벹������ʵ�鲽������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ж϶Դ�������д����������������
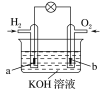
(1)������ͬ�˵����������ͬһ��Ԫ��________
(2)��ͬԪ����ɵĶ�ԭ�ӷ�����Ļ�ѧ��һ���Ǽ��Լ�________
(3)����������Ϊ2��Ԫ�ز�һ����������Ԫ��________
(4)���� 2CH3OH+3O2=2CO2+4H2O ��Ӧ ����Ƴ�ԭ���________
(5)����ȼ�ϵ�أ���ͼ��ʾ��a��b��Ϊ���Ե缫�����У�b��Ϊ�������缫��Ӧ��O2��4OH��+4e��=2H2O________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I�� ��(Sr)ԭ������Ϊ 38�������ڱ��е�λ��Ϊ_____�����ȼ��仯�����˵���в���ȷ����_________
a�� ��������ˮ���ҷ�Ӧ
b�� �ȵ�ʧ���������ȸ�ǿ
c�� Sr(OH)2 �ļ��Ա� Ca(OH)2 ��
d�� �������Ǽ���������
II���ߴ���ˮ�Ȼ��Ⱦ���(SrCl2��6H2O)���кܸߵľ��ü�ֵ��61��ʱ���忪ʼʧȥ�ᾧˮ��100��ʱʧȥȫ���ᾧˮ���ù�ҵ̼���ȷ�ĩ�������� Ba��Fe �Ļ���������ʣ��Ʊ��ߴ���ˮ�Ȼ��Ⱦ���Ĺ�������ͼ��ʾ��
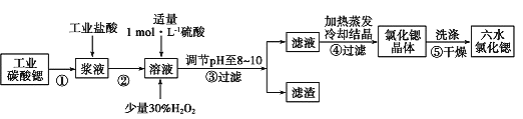
��ش�
��1����֪�����£�NaCl ��Һ��BaCl2 ��Һ�����ԣ��� MgCl2 ��CuCl2 ��Һ�����ԡ������£�SrCl2 ��Һ pH_____7��������������������������С��������
��2�������������������Ҫ�ɷ���_________���ѧʽ����������Һ pH �� 8��10����ѡ�õ��Լ�Ϊ_____��
a��ϡ���� b���������ȷ�ĩ c���������� d�������ȷ�ĩ
��3��������У�ϴ���Ȼ��Ⱦ������ѡ��_____��
a��ˮ b��ϡ���� c������������Һ d���Ȼ��ȱ�����Һ
��4����ҵ�����ȷ紵����ˮ�Ȼ��ȣ�ѡ��������¶ȷ�Χ��_____������ĸ����
a��50��60�� b��70��80�� c��80��100�� d��100������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�� a��b��c �����ڱ��е�λ����ͼ��ʾ����������Ԫ�ص����ʱȽϣ�˵����ȷ����
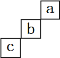
A.�ǽ�������ǿ���� a Ԫ��
B.a��b��c �ڻ������б��ֻ��ϼ���ߵ��� c
C.��̬�⻯�����ȶ����� c Ԫ��
D.����������Ӧˮ�����������ǿ���� b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ڻ�ѧ��Ӧ��ʹ��ͨ���ӱ�ɻ���������ṩ����������л�ܣ��۲���ͼ��Ȼ��ش����⡣

��ͼ�з�Ӧ��___���������������������������÷�Ӧ����H=___���ú�E1��E2�Ĵ���ʽ��ʾ����
����֪�Ȼ�ѧ����ʽ��H2(g)+![]() O2(g)=H2O(g) ��H=��241.8kJmol-1���÷�Ӧ�Ļ��Ϊ167.2kJmol-1�������淴Ӧ�Ļ��Ϊ___��
O2(g)=H2O(g) ��H=��241.8kJmol-1���÷�Ӧ�Ļ��Ϊ167.2kJmol-1�������淴Ӧ�Ļ��Ϊ___��
��2������ƽ�����ʢ��ǿ��ԭ��Һ̬�£�N2H4����ǿ������Һ̬˫��ˮ�������ǻ�Ϸ�Ӧʱ������������������ˮ���������ų��������ȡ���֪0.4molҺ̬����������Һ̬˫��ˮ��Ӧ�����ɵ�����ˮ�������ų�256.0kJ��������
�ٷ�Ӧ���Ȼ�ѧ����ʽΪ___��
������֪H2O(l)��H2O(g)����H����44kJ/mol����16gҺ̬����Һ̬˫��ˮ��Ӧ����Һ̬ˮʱ�ų�������___kJ��
�۴˷�Ӧ���ڻ���ƽ������ͷŴ����ȺͿ��ٲ������������⣬����һ���ܴ���ŵ���___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������NO�ķ�ӦΪ��![]() ��
��![]() ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��
ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��![]() ����
����![]() �¼ס��ҡ������������ܱ������У�Ͷ��
�¼ס��ҡ������������ܱ������У�Ͷ��![]() ��
��![]() ģ�ⷴӦ����ʼŨ�����±���ʾ�������жϲ���ȷ���ǣ�
ģ�ⷴӦ����ʼŨ�����±���ʾ�������жϲ���ȷ���ǣ�
��ʼŨ�� | �� | �� | �� |
|
|
|
|
|
|
|
|
A.��ʼʱ����Ӧ���ʣ���![]() ��
��![]() ��
��
B.ƽ��ʱ��![]() ����
����![]() ��
��![]() ��
��
C.ƽ��ʱ��![]() ��ת���ʣ���
��ת���ʣ���![]() ��
��
D.ƽ��ʱ������![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com