
 ,
, ;加聚;
;加聚;| 浓硫酸 |
| △ |
| 36.14 |
| 60 |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
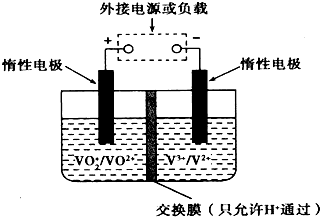 钒(V)及其化合物广泛应用于工业催化,新材料和心能源等领域.
钒(V)及其化合物广泛应用于工业催化,新材料和心能源等领域.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O2的氧化性比Fe3+强,其还原性比Fe2+强 |
| B、在H2O2分解过程中,Fe2+和Fe3+的总量保持不变 |
| C、在H2O2分解过程中,溶液的pH逐渐下降 |
| D、H2O2生产过程要严格避免混入Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
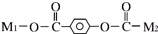 (其中M1、M2代表未知部分的结构),它在一定条件下可以发生如下转化:
(其中M1、M2代表未知部分的结构),它在一定条件下可以发生如下转化: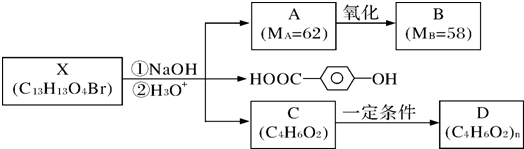
| 还原 |
| ①NaCN |
| ②H3O+ |
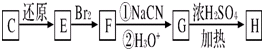
查看答案和解析>>
科目:高中化学 来源: 题型:
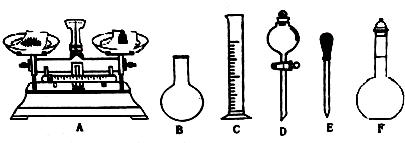
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可用加热法分离NH4Cl(s)和I2(s) |
| B、碘水中加CCl4振荡静置后,上层为紫色,下层几乎为无色 |
| C、工业上制无水酒精通常是将生石灰与95%酒精混合后蒸馏 |
| D、蒸馏、分馏和干馏都是利用组分沸点不同而分离的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验,回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验,回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com