
| A. | “春蚕到死丝方尽、蜡炬成灰泪始干”中的“丝”的主要成分是纤维素,属于天然高分子化合物 | |
| B. | “千锤万凿出深山,烈火焚烧若等闲”的过程中不但有物理变化,也有化学变化 | |
| C. | 日常生活中常用汽油去除衣物上的油污,用热的纯碱溶液洗涤炊具上的油污,两者的原理完全相同 | |
| D. | “84”消毒液的有效成分为NaClO,“洁厕灵”的有效成分为HCl,若将两者混合使用,其杀菌效果和去除厕所污渍的效果都将加强 |
分析 A.“丝”的主要成分是蛋白质;
B.千锤万凿出深山为物理变化,烈火焚烧若等闲为碳酸钙高温分解的化学反应;
C.用汽油去除衣物上的油污,为物理变化,用热的纯碱溶液洗涤炊具上的油污,与水解反应有关;
D.两者混合使用,发生氧化还原反应生成有毒气体氯气.
解答 解:A.“丝”的主要成分是蛋白质,不是纤维素,属于天然高分子化合物,故A错误;
B.千锤万凿出深山为物理变化,烈火焚烧若等闲为碳酸钙高温分解的化学反应,则过程中不但有物理变化,也有化学变化,故B正确;
C.用汽油去除衣物上的油污,为物理变化,用热的纯碱溶液洗涤炊具上的油污,与水解反应有关,分别发生萃取、盐类水解反应,原理不同,故C错误;
D.两者混合使用,发生氧化还原反应生成有毒气体氯气,则不能将二者混合使用,且杀菌效果和去除厕所污渍的效果减小,故D错误;
故选B.
点评 本题考查物质的性质、应用,为高频考点,把握物质的性质、成分及性质与应用的关系为解答的关键,侧重分析与应用能力的考查,注意判断物质组成和性质,注重元素化合物与生活相结合的训练,题目难度不大.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | -488.3 kJ/mol | B. | -244.15 kJ/mol | C. | 488.3 kJ/mol | D. | 244.15 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
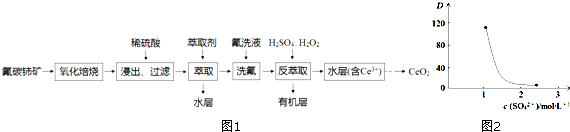
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/S | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)(×10-4mol•L-1) | 10.0 | 4.05 | 2.50 | 1.50 | 1.00 | 1.00 |
| C(CO) (×10-3mol•L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
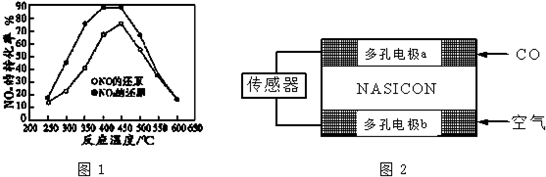
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13 | B. | 14 | C. | 15 | D. | 16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
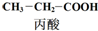 $→_{①}^{Cl_{2},红磷}$
$→_{①}^{Cl_{2},红磷}$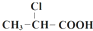 $→_{②}^{一定条件}$
$→_{②}^{一定条件}$ 下列说法正确的是( )
下列说法正确的是( )| A. | 步骤①、②分别是加成反应、取代反应 | B. | 蛋白质水解也可生成乳酸 | ||
| C. | 丙酸烃基上的二氯代物有2种 | D. | 乳酸与丙烯完全燃烧的产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
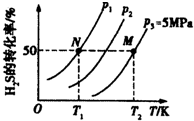 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com