
 ŅŃÖŖ£ŗpAg=-lg[c£ØAg+£©]£®Ksp£ØAgCl£©=1”Įl0-10£¬Ksp£ØAgI£©=l”Įl0-17£®ČēĶ¼ŹĒĻņl0mLAgNO3ČÜŅŗÖŠ¼ÓČė0£®lmol/LNaCIČÜŅŗŹ±£¬ČÜŅŗµÄpAgĖę׿ÓČėNaClČÜŅŗµÄĢå»ż±ä»ÆµÄĶ¼Ļó£ØŹµĻߣ©£®øł¾ŻĶ¼ĻóĖłµĆĻĀĮŠ½įĀŪÕżČ·µÄŹĒ£Ø””””£©
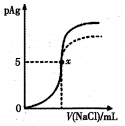
ŅŃÖŖ£ŗpAg=-lg[c£ØAg+£©]£®Ksp£ØAgCl£©=1”Įl0-10£¬Ksp£ØAgI£©=l”Įl0-17£®ČēĶ¼ŹĒĻņl0mLAgNO3ČÜŅŗÖŠ¼ÓČė0£®lmol/LNaCIČÜŅŗŹ±£¬ČÜŅŗµÄpAgĖę׿ÓČėNaClČÜŅŗµÄĢå»ż±ä»ÆµÄĶ¼Ļó£ØŹµĻߣ©£®øł¾ŻĶ¼ĻóĖłµĆĻĀĮŠ½įĀŪÕżČ·µÄŹĒ£Ø””””£©| A£® | ŌAgNO3ČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ0£®l mol/L | |
| B£® | Ķ¼ÖŠxµć±ķŹ¾ČÜŅŗÖŠc£ØAg+£©=c£ØCl-£© | |
| C£® | Ķ¼ÖŠxµćµÄ×ų±źĪŖ£Ø10£¬5£© | |
| D£® | °ŃNaClČÜŅŗ»»³É0.1 mol/LµÄMaClČÜŅŗ£¬ŌņĶ¼ĻóŌŚÖÕµćŗó±äĪŖŠéĻß²æ·Ö |
·ÖĪö A£®øł¾ŻpAg=-lg{c£ØAg+£©}Ēó³öAg+µÄÅØ¶Č£»
B£®xµćc£ØAg+£©=10-5 mol•L-1£¬Č»ŗóĄūÓĆKsp£ØAgCl£©=1”Į10-12¼ĘĖćc£ØCl-£©±Č½Ļ¼“æÉ£»
C£®xµćc£ØAg+£©=10-5 mol•L-1£¬øł¾ŻĻõĖįŅųµÄĮæĒó³öĻūŗĵÄĀČ»ÆÄĘ£»
D£®ÓÉÓŚKsp£ØAgI£©øüŠ”£¬ĖłŅŌc£ØAg+£©øüŠ”£®
½ā“š ½ā£ŗA£®Ķ¼ÖŠŌµćpAg=0£¬ŌņAg+µÄÅضČĪŖ£ŗc£ØAg+£©=100 mol•L-1£¬¼“ŌAgNO3ČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ1 mol•L-1£¬¹ŹA“ķĪó£»
B£®xµćc£ØAg+£©=10-5 mol•L-1£¬KspAgCl=1”Į10-10£¬¹Źc£ØCl-£©=$\frac{10{\;}^{-10}}{10{\;}^{-5}}$=10-5mol/L£¬¹ŹBÕżČ·£»
C£®xµćc£ØAg+£©=10-5 mol•L-1£¬Ņ»°ćČĻĪŖČÜŅŗÖŠĄė×ÓÅØ¶ČŠ”ÓŚ10-5 mol•L-1£¬¼“³ĮµķĶźČ«£¬ŌņAgNO3ÓėNaClĒ”ŗĆ·“Ó¦£¬n£ØNaCl£©=n£ØAgNO3£©=0.01L”Į1mol•L-1=0.01mol£¬ĖłŅŌV£ØNaCl£©=100mL£¬¼“xµćµÄ×ų±źĪŖ£Ø100£¬5£©£¬¹ŹC“ķĪó£»
D£®ÓėAgClĻą±Č£¬µā»ÆŅųµÄKsp£ØAgI£©øüŠ”£¬ĖłŅŌ°Ń0.1 mol•L-1µÄNaCl»»³É0.1mol•L-1NaI£¬ŌņČÜŅŗÖŠc£ØAg+£©øüŠ”£¬ŌņpAgøü“ó£¬Ķ¼Ļó²»·ū£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗB£®
µćĘĄ ±¾Ģāæ¼²éĮĖ³ĮµķµÄÉś³É¼°ČܶȻż²śŹżµÄÓ¦ÓĆ£¬×¼Č·°ŃĪÕĶ¼Ļóŗ¬Ņ唢°ŃĪÕĢāøÉÖŠµÄŠÅĻ¢£¬ŹģĻ¤ČܶȻż¹ęŌņŹĒ½āĢā¹Ų¼ü£¬æ¼²éѧɜ·ÖĪöĢāÄæŠÅĻ¢²¢ÓĆÓŚ½ā¾öĪŹĢāµÄÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2.3 gNa+ÖŠŗ¬ÓŠNAøöµē×Ó | |
| B£® | ĮņĖįµÄĦ¶ūÖŹĮæÓėĮņĖį·Ö×ÓµÄÖŹĮæĻąµČ | |
| C£® | NAøöCC14·Ö×ÓŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ĪŖ22.4 L | |
| D£® | 18 g H2OÖŠŗ¬ÓŠNAøöH2”¢NAøöO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ł¢Ū¢Ü | D£® | ¢Ł¢Ś¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
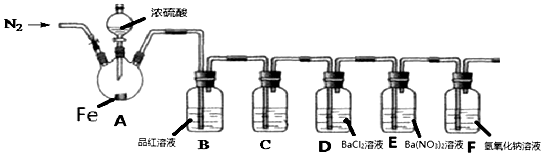
 ŅŃÖŖA”¢B”¢C”¢D”¢E¶¼ŹĒÖÜĘŚ±ķÖŠĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£®ĘäÖŠAŌŖĖŲŌ×ÓµÄŗĖĶāpµē×ÓŹż±Čsµē×ÓŹżÉŁ1£®CŹĒµēøŗŠŌ×ī“óµÄŌŖĖŲ£®DŌ×Ó“ĪĶā²ćµē×ÓŹżŹĒ×īĶā²ćµē×ÓŹż2±¶£¬EŹĒµŚ¢ų×åÖŠŌ×ÓŠņŹż×īŠ”µÄŌŖĖŲ£®
ŅŃÖŖA”¢B”¢C”¢D”¢E¶¼ŹĒÖÜĘŚ±ķÖŠĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£®ĘäÖŠAŌŖĖŲŌ×ÓµÄŗĖĶāpµē×ÓŹż±Čsµē×ÓŹżÉŁ1£®CŹĒµēøŗŠŌ×ī“óµÄŌŖĖŲ£®DŌ×Ó“ĪĶā²ćµē×ÓŹżŹĒ×īĶā²ćµē×ÓŹż2±¶£¬EŹĒµŚ¢ų×åÖŠŌ×ÓŠņŹż×īŠ”µÄŌŖĖŲ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŹµŃé | ĻņŹŌ¹ÜÖŠ¼ÓČė2mlČÜŅŗ | ŹµŃéĻÖĻó |
 | ŹµŃé¢ń£ŗ0.5mol/LCuCl2ČÜŅŗ | 15s£ŗ“óĮæĘųÅŻĒŅÓŠŗģÉ«ĪļÖŹĪö³ö 60s£ŗ·“Ó¦½ųŅ»²½¼ÓæģĒŅ·“Ó¦¾ēĮŅ·ÅČČ£¬ŅŗĢå¼øŗõ·ŠĢŚ 120s£ŗĀĮʬ·“Ó¦Ķź£¬ŹŌ¹ÜÖŠĪö³ö“óĮæÅīĖɵÄŗģÉ«ĪļÖŹ |
| ŹµŃé¢ņ£ŗ0.5mol/LCuSO4ČÜŅŗ | 15s ĪŽĆ÷ĻŌĻÖĻó 60s£ŗĀĮʬ±ķĆęÓŠ¼«ÉŁĘųÅŻ 120s£ŗÓŠÉŁĮæĘųÅŻŅē³ö£¬ĀĮʬ±ßŌµÓŠŗÜÉŁŗģÉ«ĪļÖŹÉś³É |
| ŹµŃé | ĻņŹŌ¹ÜÖŠ¼ÓČė2mLČÜŅŗ | ŹµŃéĻÖĻó |
 | ŹµŃé¢ó£ŗ0.5mol/LCuCl2ČÜŅŗ+1g Na2SO4¹ĢĢå | ¼ÓČė Na2SO4¹ĢĢåŗóĖŁĀŹ¼øŗõ²»±ä£¬ČŌÓŠ“óĮæĘųÅŻ²śÉś£¬ŗģÉ«ĪļÖŹÉś³ÉĒŅ¾ēĮŅ·ÅČČ£¬ĀĮʬ·“Ó¦ĶźČ«£¬ČÜŅŗ·ŠĢŚ |
| ŹµŃé¢ō£ŗ0.5mol/L CuCl2ČÜŅŗ+5g Na2SO4¹ĢĢå | ¼ÓČėNa2SO4¹ĢĢåŗóĖŁĀŹ¼øŗõ²»±ä£¬ČŌÓŠ“óĮæĘųÅŻ²śÉś£¬ŗģÉ«ĪļÖŹÉś³ÉĒŅ¾ēĮŅ·ÅČČ£¬ĀĮʬ·“Ó¦ĶźČ«£¬ČÜŅŗ·ŠĢŚ | |
| ŹµŃé¢õ£ŗ0.5mol/LCuSO4ČÜŅŗ+0.02mol NaCl¹ĢĢå | Ī“¼ÓČė NaCl¹ĢĢåĒ°¼øŗõĆ»ĻÖĻ󣬼ÓČėŗó£¬ĀĮʬ±ķĆęŃøĖŁ²śÉś“óĮæĘųĢåŗĶŗģÉ«ĪļÖŹ£¬ČÜŅŗĪĀ¶ČÉĻÉżÖĮ·ŠĢŚ£¬ĀĮ·“Ó¦ĶźČ« | |
| ŹµŃé¢ö£ŗ0.5mol/LCuSO4ČÜŅŗ+0.02mol NH4Cl¹ĢĢå | Ī“¼ÓČė NH4Cl¹ĢĢåĒ°¼øŗõĆ»ĻÖĻ󣬼ÓČėŗó£¬ĀĮʬ±ķĆęŃøĖŁ²śÉś“óĮæĘųĢåŗĶŗģÉ«ĪļÖŹ£¬ČÜŅŗĪĀ¶ČÉĻÉżÖĮ·ŠĢŚ£¬ĀĮ·“Ó¦ĶźČ« |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com