
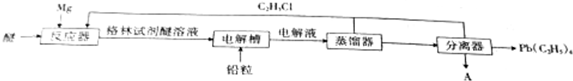
 £¬µē½āĪļÖŹAµÄ»Æѧ·½³ĢŹ½ĪŖMgCl2$\frac{\underline{\;µē½ā\;}}{\;}$Mg+Cl2”ü£®
£¬µē½āĪļÖŹAµÄ»Æѧ·½³ĢŹ½ĪŖMgCl2$\frac{\underline{\;µē½ā\;}}{\;}$Mg+Cl2”ü£®·ÖĪö £Ø1£©Ć¾ŗĶ¶žŃõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ŗĶŃõ»ÆĆ¾£¬ÓĆĆ¾Š¼“śĢęĆ¾æ飬æÉŅŌŌö“ó·“Ó¦Īļ½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ£¬µ«·“Ó¦ĖŁĀŹ²»ÄÜĢ«æģĒŅĆ¾·ŪŌŚæÕĘųÖŠČŻŅ×±»ŃõĘųŃõ»Æ£¬ĖłŅŌ²»ŅĖÓĆĆ¾·Ū£»
£Ø2£©Ńō¼«²ĪÓėµē¼«·“Ó¦µÄŹĒøńĮÖŹŌ¼ĮŗĶĒ¦£¬ŹĒĒ¦Ź§Č„µē×ÓÉś³ÉPb£ØC2H5£©4£¬øł¾ŻŌŖĖŲŹŲŗćŗĶµēŗÉŹŲŗćŹéŠ“µē¼«·“Ó¦Ź½£»
£Ø3£©øł¾ŻŌŖĖŲŹŲŗćŗĶµēŗÉŹŲŗćæÉÖŖ£¬µē½ā²ŪÖŠ·¢ÉśµÄ·“Ó¦ĪŖPb+4C2H5MgCl$\frac{\underline{\;µē½ā\;}}{\;}$Pb£ØC2H5£©4+2Mg+2MgCl2£¬ĖłŅŌ“Ó·ÖĄėĘ÷ÖŠ·ÖĄė³öĄ“µÄĪļÖŹAĪŖMgCl2£¬µē½āMgCl2Éś³ÉĆ¾ŗĶĀČĘų£»
£Ø4£©øł¾Ż·“Ó¦C2H5Cl+Mg$\stackrel{ĪŽĖ®ŅŅĆŃ}{”ś}$C2H5MgCl”¢Pb+4C2H5MgCl$\frac{\underline{\;µē½ā\;}}{\;}$Pb£ØC2H5£©4+2Mg+2MgCl2£¬æÉÖŖæŖŹ¼Ķ¶ČėµÄPbŗĶMgµÄĪļÖŹµÄĮæÖ®±Č£»
£Ø5£©ĖÄŅŅ»łĒ¦Č¼ÉÕ¼“ÓėŃõĘų·“Ӧɜ³ÉÉś³ÉŅ»Ńõ»ÆĒ¦”¢¶žŃõ»ÆĢ¼ŗĶĖ®£¬øł¾ŻŌŖĖŲŹŲŗćŹéŠ“»Æѧ·½³ĢŹ½£»
½ā“š ½ā£ŗ£Ø1£©Ć¾ŗĶ¶žŃõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ŗĶŃõ»ÆĆ¾£¬·“Ó¦·½³ĢŹ½ĪŖCO2+2Mg$\frac{\underline{\;µćČ¼\;}}{\;}$C+2MgO£¬ÓĆĆ¾Š¼“śĢęĆ¾æ飬æÉŅŌŌö“ó·“Ó¦Īļ½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ£¬µ«·“Ó¦ĖŁĀŹ²»ÄÜĢ«æģĒŅĆ¾·ŪŌŚæÕĘųÖŠČŻŅ×±»ŃõĘųŃõ»Æ£¬ĖłŅŌ²»ŅĖÓĆĆ¾·Ū£¬
¹Ź“š°øĪŖ£ŗCO2+2Mg$\frac{\underline{\;µćČ¼\;}}{\;}$C+2MgO£»Ōö“ó·“Ó¦Īļ½Ó“„Ć껿£¬¼Óæģ·“Ó¦ĖŁĀŹ£»ÓĆĆ¾·Ū·“Ó¦ĖŁĀŹĢ«æģĒŅĆ¾·ŪŌŚæÕĘųÖŠČŻŅ×±»ŃõĘųŃõ»Æ£»
£Ø2£©Ńō¼«²ĪÓėµē¼«·“Ó¦µÄŹĒøńĮÖŹŌ¼ĮŗĶĒ¦£¬ŹĒĒ¦Ź§Č„µē×ÓÉś³ÉPb£ØC2H5£©4£¬Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖPb-4e-+4C2H5MgCl=Pb£ØC2H5£©4+4Mg2++4Cl-£¬
¹Ź“š°øĪŖ£ŗPb-4e-+4C2H5MgCl=Pb£ØC2H5£©4+4Mg2++4Cl-£»
£Ø3£©øł¾ŻŌŖĖŲŹŲŗćŗĶµēŗÉŹŲŗćæÉÖŖ£¬µē½ā²ŪÖŠ·¢ÉśµÄ·“Ó¦ĪŖPb+4C2H5MgCl$\frac{\underline{\;µē½ā\;}}{\;}$Pb£ØC2H5£©4+2Mg+2MgCl2£¬ĖłŅŌ“Ó·ÖĄėĘ÷ÖŠ·ÖĄė³öĄ“µÄĪļÖŹAĪŖMgCl2£¬Ęäµē×ÓŹ½ĪŖ£ŗ £¬µē½āMgCl2Éś³ÉĆ¾ŗĶĀČĘų£¬·“Ó¦·½³ĢŹ½ĪŖMgCl2$\frac{\underline{\;µē½ā\;}}{\;}$Mg+Cl2”ü£¬
£¬µē½āMgCl2Éś³ÉĆ¾ŗĶĀČĘų£¬·“Ó¦·½³ĢŹ½ĪŖMgCl2$\frac{\underline{\;µē½ā\;}}{\;}$Mg+Cl2”ü£¬
¹Ź“š°øĪŖ£ŗ £»MgCl2$\frac{\underline{\;µē½ā\;}}{\;}$Mg+Cl2”ü£»
£»MgCl2$\frac{\underline{\;µē½ā\;}}{\;}$Mg+Cl2”ü£»
£Ø4£©øł¾Ż·“Ó¦C2H5Cl+Mg$\stackrel{ĪŽĖ®ŅŅĆŃ}{”ś}$C2H5MgCl”¢Pb+4C2H5MgCl$\frac{\underline{\;µē½ā\;}}{\;}$Pb£ØC2H5£©4+2Mg+2MgCl2£¬æÉÖŖæŖŹ¼Ķ¶ČėµÄPbŗĶMgµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ4£¬
¹Ź“š°øĪŖ£ŗ1£ŗ4£»
£Ø5£©ĖÄŅŅ»łĒ¦Č¼ÉÕ¼“ÓėŃõĘų·“Ӧɜ³ÉÉś³ÉŅ»Ńõ»ÆĒ¦”¢¶žŃõ»ÆĢ¼ŗĶĖ®£¬·“Ó¦»Æѧ·½³ĢŹ½ĪŖ2Pb£ØC2H5£©4+27O2$\frac{\underline{\;µćČ¼\;}}{\;}$2PbO+16CO2+20H2O£¬
¹Ź“š°øĪŖ£ŗ2Pb£ØC2H5£©4+27O2$\frac{\underline{\;µćČ¼\;}}{\;}$2PbO+16CO2+20H2O£»
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĮĖĪļÖŹÖʱøŹµŃ飬Éę¼°·½³ĢŹ½µÄŹéŠ“”¢µē¼«·“Ó¦Ź½µÄŹéŠ“”¢µē×ÓŹ½µČ£¬ÕżČ·Ąķ½āĮ÷³ĢŹĒ½āĢā¹Ų¼ü£¬“šĢāŹ±×¢ŅāÓ¦ÓĆŌŖĖŲŹŲŗć ŗĶµēŗÉŹŲŗćµÄĖ¼Ļė£¬ĢāÄæÄѶČÖŠµČ£¬²ąÖŲ»Æѧ»ł“”ÖŖŹ¶ŗĶ»ł±¾ÄÜĮ¦µÄ漲飮



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | N2 | B£® | NH3 | C£® | CO2 | D£® | CH4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
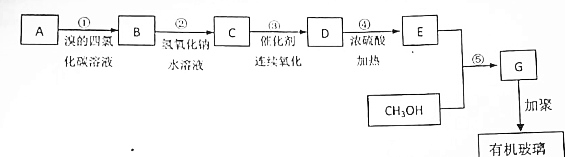
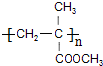 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
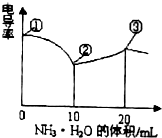
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| t/min | 0 | 20 | 40 | 60 | 80 |
| c£ØH2O2£©/mol•L-1 | 1.0 | 0.60 | 0.40 | 0.20 | 0.10 |
| ĻÖĻó | ½įĀŪ | |
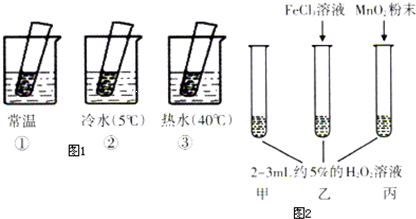
| ČČĖ®ÖŠ | ČÜŅŗÖŠÓŠĘųÅŻ²śÉś£¬±Č³£ĪĀæģ | ÉżøßĪĀ¶Č£¬H2O2µÄ·Ö½āĖŁĀŹ¼Óæģ |
| ³£ĪĀÖŠ | ČÜŅŗÖŠÓŠĘųÅŻ²śÉś£¬ĒŅĖŁ¶Č½Ļæģ | ĪŽ |
| ĄäĖ®ÖŠ | ČÜŅŗÖŠÓŠĘųÅŻ²śÉś£¬±Č³£ĪĀĀż | ½µµĶĪĀ¶Č£¬H2O2µÄ·Ö½āĖŁĀŹ¼õĀż |
| ĻÖĻó | ½įĀŪ | |
| ±ū¼ÓČėMnO2 | MnO2ÄܼÓæģ»Æѧ·“Ó¦ĖŁĀŹ | |
| ŅŅ¼ÓČėFeCl3 | FeCl3ÄܼÓæģ»Æѧ·“Ó¦ĖŁĀŹ | |
| ¼×²»¼ÓĘäĖūŹŌ¼Į | ČÜŅŗÖŠÓŠÉŁĮæĘųÅŻ³öĻÖ | ²»Ź¹ÓĆ“ß»Æ¼Į»Æѧ·“Ó¦ĖŁĀŹ½ĻŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaAlO2 ŗĶ HCl | B£® | MgCl2ŗĶ NH3•H2O | C£® | Na2CO3ŗĶHCl | D£® | AlCl3ŗĶNaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±łÕņµÄĘ”¾Ę“ņæŖŗó·ŗĘšÅŻÄ | |
| B£® | 500”ę×óÓŅ±ČŹŅĪĀøüÓŠĄūÓŚŗĻ³É°±µÄ·“Ó¦£Ø”÷H£¼0£© | |
| C£® | ŗģ×ŲÉ«µÄNO2¼ÓŃ¹ŗóŃÕÉ«ĻȱäÉīŌŁ±äĒ³£Ø2 NO2?N2O4£ØĪŽÉ«£©£© | |
| D£® | ¹āÕÕŠĀÖʵÄĀČĖ®Ź±£¬ČÜŅŗµÄpHÖš½„¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4LH2Oŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ1 NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬1molNa2CO3ŗ¬ÓŠµÄNa+Ąė×ÓŹżĪŖ2 NA | |
| C£® | Ķس£×“æöĻĀ£¬1 NA øöCO2·Ö×ÓÕ¼ÓŠµÄĢå»żĪŖ22.4L | |
| D£® | 1mol/LµÄMgCl2ČÜŅŗÖŠ£¬ŗ¬ÓŠCl- øöŹżĪŖ2 NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com