
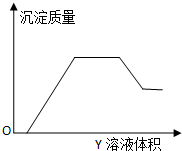
 向X溶液中缓慢滴加Y溶液,生成沉淀的质量如图所示,表中符合图象的一组是( )
向X溶液中缓慢滴加Y溶液,生成沉淀的质量如图所示,表中符合图象的一组是( )| X | Y | |
| A | AlCl3、Mg(NO3)2、HNO3 | NaOH |
| B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 |
| C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH |
| D | NaAlO2、氨水、NaOH | H2SO4 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、向Al2(SO4)3溶液中加过量的NaOH溶液可制备Al(OH)3 |
| B、将过量的过氧化钠投入FeCl2溶液中,最终看到白色沉淀 |
| C、用稀硫酸清洗做焰色反应的铁丝 |
| D、镁合金的硬度和强度均高于纯镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液呈中性 |
| B、该溶液中:2c(Al3+)+c(Fe2+)+c(H+)=4c(SO42-)+c(OH-) |
| C、在空气中蒸干并灼烧该溶液,最后所得残留固体为氧化铝和氧化铁 |
| D、向该溶液中加入氢氧化钡溶液,当SO42-完全沉淀是,Al3+、Fe2+恰好被完全沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| HCl |
| X |
| A、NH3?H2O |
| B、CO2 |
| C、NaOH |
| D、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:3 | B、3:1 |
| C、3:2 | D、1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、CO2是氧化产物 |
| B、H2C2O4在反应中被氧化 |
| C、1mol H2C2O4参加反应,转移的电子为1mol |
| D、H2C2O4的氧化性强于ClO2的氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com