
| ŅŅ“¼ |
| ”÷ |
| ŅŅ“¼ |
| ”÷ |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
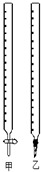
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ŅŃÖŖX”¢Y”¢Z”¢W”¢QŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĪåÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£®ĘäÖŠÖ»ÓŠZŹĒ½šŹō£¬WµÄÖŹ×ÓŹżŹĒYµÄ2±¶£¬X”¢Y”¢WŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆ¹ŲĻµČēĶ¼£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ŅŃÖŖX”¢Y”¢Z”¢W”¢QŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĪåÖÖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£®ĘäÖŠÖ»ÓŠZŹĒ½šŹō£¬WµÄÖŹ×ÓŹżŹĒYµÄ2±¶£¬X”¢Y”¢WŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆ¹ŲĻµČēĶ¼£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A”¢ĪåÖÖŌŖĖŲÖŠŌ×Ó°ė¾¶×ī“óµÄŹĒX£¬Ąė×Ó°ė¾¶×ī“óµÄŹĒQĄė×Ó |
| B”¢ĪåÖÖŌŖĖŲÖŠQµÄ×īøß¼ŪŃõ»ÆĪļĖł¶ŌÓ¦µÄĖ®»ÆĪļµÄĖįŠŌ×īĒæ |
| C”¢YÓėZŠĪ³ÉµÄ»ÆŗĻĪļŅ»¶ØŹĒ¼īŠŌŃõ»ÆĪļ |
| D”¢ZÓėQŠĪ³ÉµÄ»ÆŗĻĪļĖ®ČÜŅŗŅ»¶ØĻŌĖįŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢Fe£ØOH£©3ČÜÓŚĒāµāĖįÖŠ£ŗFe£ØOH£©3+3H+=Fe3++3H2O |
| B”¢Ģ¼ĖįĒāÄĘČÜŅŗÓė¹żĮæ³ĪĒåŹÆ»ŅĖ®·“Ó¦£ŗHCO3-+Ca2++OH-=CaCO3”ż+H2O |
| C”¢ĮņĖįŃĒĢśČÜŅŗÖŠ¼ÓČėĖį»ÆµÄĖ«ŃõĖ®£ŗFe2++2H++H2O2=Fe3++2H2O |
| D”¢ĻņĆ÷·ÆČÜŅŗÖŠµĪ¼Ó¹żĮæ°±Ė®£ŗAl3++4NH3?H2OØTAlO2-+4NH4++2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ÓĆ0.1320mol/LµÄHClČÜŅŗµĪ¶ØĪ“ÖŖÅØ¶ČµÄNaOHČÜŅŗ£¬ŹµŃ鏿¾ŻČēĻĀ±ķĖłŹ¾£¬
ÓĆ0.1320mol/LµÄHClČÜŅŗµĪ¶ØĪ“ÖŖÅØ¶ČµÄNaOHČÜŅŗ£¬ŹµŃ鏿¾ŻČēĻĀ±ķĖłŹ¾£¬| ŹµŃ鱹ŗÅ | “ż²āNaOHČÜŅŗµÄĢå»ż/mL | HClČÜŅŗµÄĢå»ż/mL |
| 1 | 25.00 | 24.41 |
| 2 | 25.00 | 24.39 |
| 3 | 25.00 | 22.60 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
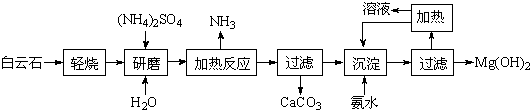
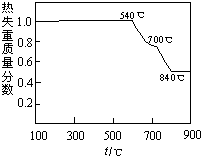
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
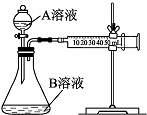 ŹµŃ銔×éĄūÓĆĖįŠŌKMnO4ČÜŅŗÓėH2C2O4ČÜŅŗ·“Ӧъ¾æÓ°Ļģ·“Ó¦ĖŁĀŹµÄŅņĖŲ£®
ŹµŃ銔×éĄūÓĆĖįŠŌKMnO4ČÜŅŗÓėH2C2O4ČÜŅŗ·“Ӧъ¾æÓ°Ļģ·“Ó¦ĖŁĀŹµÄŅņĖŲ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ŹµŃé·½°ø £ØÖ»ŅŖĒóĢīŠ“Ń”ÓĆŹŌ¼ĮµÄŠņŗÅ£© | ŹµŃéĻÖĻó | ½įĀŪ | |
| £Ø1£© | Ņ»Ö§ŹŌ¹ÜÖŠÓŠ°×É«³Įµķ£¬ĮķŅ»Ö§ŹŌ¹ÜÖŠĻČÉś³É°×É«³Įµķ£¬ŗó°×É«³ĮµķĻūŹ§£® | ½šŹōŠŌ£ŗMg£¾Al | |
| £Ø2£© | ·Ē½šŹōŠŌ£ŗ | ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com