
| A. | ①③④⑤⑥⑦ | B. | ②③④⑤ | C. | ①②④⑤⑥⑦ | D. | 全部 |
科目:高中化学 来源: 题型:多选题
| X | Y | W | Z | 反应体系能量变化 | |
| 甲 | 2mol | 1mol | 放出akJ/mol | ||
| 乙 | 1mol | 1mol | 放出b kJ/mol | ||
| 丙 | 2mol | 2mol | 放出c kJ/mol | ||
| 丁 | 3mol | 2mol | 吸收d kJ/mol |
| A. | c+d<Q | |
| B. | 平衡时,甲、丁容器中X、W的转化率之和等于1 | |
| C. | 平衡时丙容器中Z的物质的量浓度最大 | |
| D. | X的转化率为:甲<乙<丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有羟基的化合物一定属于醇类 | |
| B. | 酚和醇都含有羟基,但其化学性质不完全相同 | |
| C. | 分子中含有苯环和羟基的化合物一定是酚 | |
| D. | Na2SO3、Na2O2、苯酚久置于空气中,颜色均有变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子最外层电子数比B原子最外层电子数少 | |
| B. | A的最高价氧化物对应水化物的碱性强于B的最高价氧化物对应水化物的碱性 | |
| C. | 1molA与足量酸反应生成的H2比1molB与足量酸反应生成的H2多 | |
| D. | 常温时,A、B均能导电,且导电性良好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
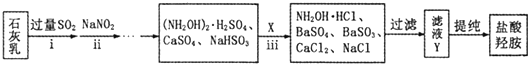
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A组 | B组 |
| Ⅰ.H-F键的键能大于H-O键的键能 | ①HF的沸点比H2O低 |
| Ⅱ.H-H…F氢键的键能大于O-H…O氢键的键能 | ②HF比H2O稳定 |
| Ⅲ.HF分子间能形成的氢键个数比H2O分子少 | ③HF的沸点比H2O高 |
| Ⅳ.HF分子与水分子可形成氢键 | ④HF极易溶于水 |
| A. | I② | B. | Ⅱ③ | C. | Ⅲ① | D. | Ⅲ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com