
【题目】有机物a和苯通过反应合成b的过程可表示为如图(无机小分子产物略去)。下列说法错误的是
![]()
A. 该反应是取代反应
B. 若R为—CH3时,b中所有原子共面
C. 若R为—C4H9时,则b中苯环上的一氯代物可能的结构共有12种
D. 若R为—C4H5O时,1mol b最多可以与5molH2加成
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒。某兴趣小组进行下面实验探究,查阅资料知道:① HNO2为弱酸,② 2NO + Na2O2 = 2NaNO2,③ 2NO2 + Na2O2 = 2NaNO3 ④ 酸性KMnO4溶液可将NO和NO2-均氧化为NO3-,MnO4-还原成Mn2+。NaNO2的制备方法可有如下2种方法(夹持装置和加热装置已略,气密性已检验):
制备装置1:
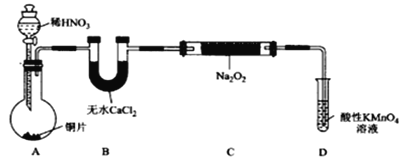
制备装置2:
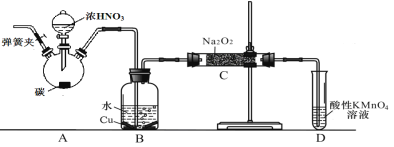
(1)在制备装置1中:
①如果没有B装置,C中发生的副反应有_________;
②甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质;于是在A装置与B装置间增加了_____装置,改进后提高了NaNO2的纯度;
③ D装置发生反应的离子方程式为______。
(2)在制备装置2中:
① B装置的作用是_______________________;
②写出装置A烧瓶中发生反应的化学方程式并用单线桥标出电子的转移___________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是一种自然界分布较广的元素,在很多化合物中都含有该元素,回答下列问题:
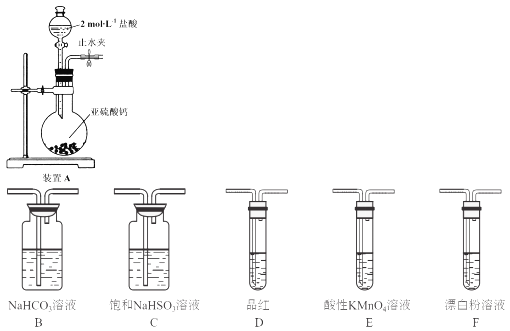
(1)装置A中反应的化学方程式为___________。
(2)使分液漏斗中液体顺利流下的操作是___________。
(3)选用上面的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F的顺序连接装置即可证明,乙同学认为该方案不合理,其理由是___________。
②丙同学设计的合理实验方案为:A→C→_____→___→D→F,其中装置C的作用是_____,证明亚硫酸的酸性强于次氯酸的实验现象是____。
(4)K2S2O3具有强氧化性,可通过电解H2SO4和K2SO4的混合溶液制得,其阳极反应式为_____。称取0.2500g产品于碘量瓶中,加100mL水溶解,再加入8.000g KI固体(稍过量),振荡使其充分反应;加入适量醋酸溶液酸化,以淀粉为指示剂,用cmol/L的Na2S2O3标准液滴定至终点,消耗Na2S2O3标准液VmL,则样品中K2S2O8的纯度为______%(用含c、V的代数式表示,已知:S2O82-+2I-=2SO42-+I2;2S2O32-+I2=S4O62-+2I-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是:
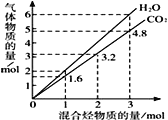
①一定有乙烯 ②一定有甲烷 ③一定有丙烷 ④一定没有乙烷⑤可能有甲烷 ⑥可能有乙炔(C2H2)
A. ②④ B. ②③⑥ C. ②⑥ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置完成对应的实验(部分仪器略去),能达到实验目的的是

A. 利用A装置制取乙酸乙酯B. 利用B装置吸收氨气
C. 利用C装置在实验室里制取乙烯D. 利用D装置比较盐酸、碳酸、苯酚的酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BHT是一种常用的食品抗氧化剂,从![]() 出发合成BHT的方法有如下两种。下列说法错误的是
出发合成BHT的方法有如下两种。下列说法错误的是
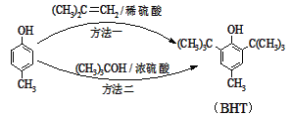
A. 从绿色化学角度分析方法一优于方法二
B. 推测BHT在水中的溶解度小于苯酚
C. BHT与![]() 都能使酸性KMnO4褪色
都能使酸性KMnO4褪色
D. 方法一的反应类型是取代反应,方法二的反应类型是加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列几组物质中,互为同位素的有__________,互为同素异形体的有__________,互为同系物的有__________,互为同分异构体的有__________,属于同种物质的__________。
①O2和O3 ②35Cl和37Cl③CH3CH3和CH3CH2CH3④CH3CH2CH(CH3)CH2CH3和CH3CH2CH(CH3)CH(CH3)CH3
⑤H2、D2和T2⑥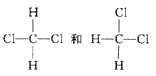 ⑦CH3(CH2)2CH3和(CH3)2CHCH3 ⑧CH3CH(CH3)CH和CH(CH3)3
⑦CH3(CH2)2CH3和(CH3)2CHCH3 ⑧CH3CH(CH3)CH和CH(CH3)3
(2)含有10个及10个以下碳原子的烷烃,其一氯代物只有一种的共有4种,请写出这4种烷烃的结构简式和名称:_______、_______、______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈及其化合物在工业生产中应用广泛。以某玻璃废料(主要成分为CeO2、SiO2、Fe2O3、FeO等)为原料制备CeO2和NH4Fe(SO4)2·12H2O(硫酸铁铵晶体),其流程如下(已知CeO2既不溶于稀硫酸,也不溶于氢氧化钠溶液):
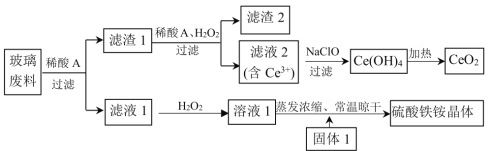
回答下列问题:
(1)浸取玻璃废料选用的“稀酸A”为____________(填“稀硫酸”或“稀盐酸”)。
(2)向滤渣1加入H2O2的目的是_________(用离子方程式表示)。为了提高溶解“滤渣1”的速率,常釆用加热措施,但温度高于60℃时溶解速率减慢,其主要原因是____________。
(3)为了不引入杂质,所选用固体1的化学式为_______________。
(4)制备2mol CeO2需要NaClO的质量为____________。
(5)锌铈液流电池放电时的工作原理如图所示。
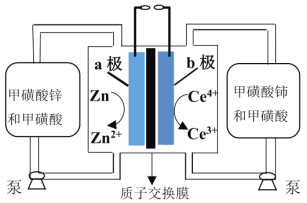
①放电时电池的总离子反应方程式为____________________。
②充电时,当a极增重6.5g时,有_________mol离子通过交换膜以平衡电荷。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是
A. 气态氢化物的稳定性:H2O>NH3
B. 钠元素的金属性比镁元素的强
C. 图所示实验可证明元素的非金属性:Cl>C>Si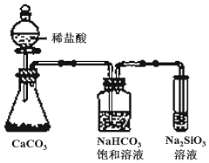
D. 在元素周期表中金属和非金属的分界处可以找到半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com