
| ��ѧʽ | ���볣�� |
| HF | Ki=3.5��10-4 |
| H2CO3 | Ki1=4.3��10-7 |
| Ki2=5.6��10-11 | |
| HClO | Ki=3.2��10-8 |
| A�� | ͬ��ͬŨ���£���Һ��pHֵ��NaF��NaClO��Na2CO3 | |
| B�� | ���H+��������ClO-��HCO3-��F- | |
| C�� | ����������Һ��ͨ����������̼�����ӷ���ʽ��ClO-+CO2+H2O��HCO3-+HClO | |
| D�� | ̼������Һ�м����������������ӷ���ʽ��CO32-+2HF��2F-+H2O+CO2�� |
���� ����ĵ���ƽ�ⳣ��Խ������Խǿ������ĵ���ƽ�ⳣ��ԽС������Խ�������Ӧ����ˮ��̶�Խ�ݱ������ƽ�ⳣ����֪��������ǿ������˳��Ϊ��HF��H2CO3��HClO��ǿ���ܹ���ȡ���ᣬ�ݴ˽��н��
��� �⣺�ݱ��������������ǿ������˳��Ϊ��HF��H2CO3��HClO��
A��������ǿ������˳��Ϊ��HF��H2CO3��HClO������Խ�����������������ӵ�����Խǿ����ҺpH��СΪ��Na2CO3��NaClO��NaF����A����
B��������ǿ������˳��Ϊ��HF��H2CO3��HClO�����H+��������ClO-��HCO3-��F-����B��ȷ��
C��̼��ĵ�һ���������Աȴ�����ǿ�����Է�����Ӧ��ClO-+CO2+H2O=HCO3-+HClO����C��ȷ��
D��̼������Һ�м������������ʱ��������̼��������ӣ����ӷ���ʽΪ��CO32-+HF=F-+HCO3-����D����
��ѡBC��
���� ���⿼����������ʵĵ���ƽ�⼰��Ӱ�죬��Ŀ�Ѷ��еȣ����ݵ���ƽ�ⳣ����ȷ�ж�����ǿ��Ϊ���ؼ���ע������Ӱ�����ƽ�⡢�ε�ˮ������أ�����������ѧ�����������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ������������Ӧ���鲻�� | |
| B�� | ��ϩ�;���ϩ����ʹ������Ȼ�̼��Һ��ɫ | |
| C�� | ��ϩ�ͱ�����ʹ���Ը��������Һ��ɫ | |
| D�� | ��ϩ�����鶼���Է���������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��С��Mg��S��O��F | |
| B�� | �����������������ȣ�P��S��Cl | |
| C�� | ��ɢ����ֱ����С��Fe��OH��3���壾CaCO3����Һ��NaCl��Һ | |
| D�� | ����ǿ����H2SO4��H3PO4��H2SiO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
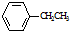 $��_{����}^{Fe_{2}O_{2}}$
$��_{����}^{Fe_{2}O_{2}}$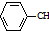 =CH2+H2������˵����ȷ���ǣ�������
=CH2+H2������˵����ȷ���ǣ�������| A�� | �������Ը��������Һ�����ұ��ͱ���ϩ | |
| B�� | �ұ�������ϩ��ʹ��ˮ��ɫ��ԭ�������߷�����������Ӧ | |
| C�� | �÷�Ӧ�ķ�Ӧ����Ϊ��ȥ��Ӧ | |
| D�� | �ұ��ͱ���ϩ�����ڹ�ƽ���̼ԭ��������Ϊ7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
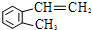 ����һ����Ҫ���л�����ԭ�ϣ�
����һ����Ҫ���л�����ԭ�ϣ�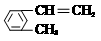 ��
��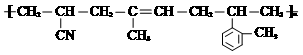 �����谴1��1��1�ĵ�������ϳɣ���
�����谴1��1��1�ĵ�������ϳɣ���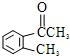 ��д����صĻ�ѧ����ʽ��
��д����صĻ�ѧ����ʽ��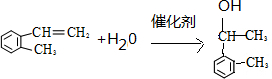 ��
��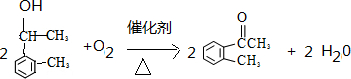 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Mg2+�ĵ����Ų�ʽ��1s22s22p63s2 | B�� | �����Ŀռ�ṹ�������� | ||
| C�� | Na2S�ĵ���ʽ��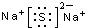 | D�� | ��ȩ�Ľṹ��ʽ��CH2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| ���� | Na2CO3��NaHCO3�� | CO2��HCl�� | FeCl2��FeCl3�� | CO2��SO2�� |
| �����Լ� | ����ʯ��ˮ | ����Na2CO3��Һ | ���� | ����NaHSO3��Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ó����е�ʳ�׳�ȥ��ˮƿˮ���е�CaCO3��CaCO3+2H+=Ca2++CO2��+H2O | |
| B�� | ��NH4HCO3��Һ�мӹ�����NaOH��Һ�����ȣ�NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O | |
| C�� | �����Ե⻯����Һ�еμ�������˫��ˮ��2I-+2H++H2O2=I2+2H2O | |
| D�� | Cl2ͨ��ˮ�У�Cl2+H2O?2H++Cl-+ClO- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com