
【题目】将铜加入一定量稀硫酸和过氧化氢混合溶液中,充分反应后,溶液呈蓝色,有无色气体产生;若还发现容器底部有少量固体,则该固体可能是( )
A.Cu
B.S
C.CuS
D.Cu2S
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤:
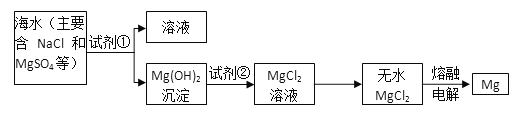
试回答下列问题:
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用__________________________;
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是____________________;
(3)试剂②可以选用_______;反应的离子方程式为:__________________________;
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,写出该反应的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A是合成天然橡胶的单体,分子式为C5H8。A的一系列反应如图(部分反应条件略去)
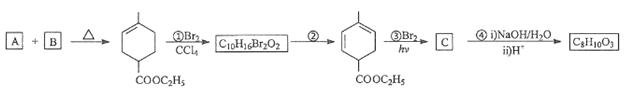
已知:(1)![]()
(2)CH3COOCH2CH3+H2O![]() CH3COOH+CH3CH2OH
CH3COOH+CH3CH2OH
回答下列问题:
(1)A的结构简式为_______。
(2)B的分子式为_______。
(3)②的反应方程式为_______。
(4)①和③的反应类型分别是_____, ______。
(5)C为单溴代物,分子中有两个亚甲基,其结构简式为__________。
(6)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的共轭二烯烃与单烯径都可发生类似A和B之间的反应。请写出均为六元环烃的M(C6H10)与N(C6H8)发生该类反应的化学方程式____________________。
(7)A的同分异构体中不含累积二烯(C=C=C)结构单元的链状经还有_______种(不考虑顺反异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法不正确的是
A.过氧化钠可用作潜水艇中的供氧剂 B.氧化铝可用于制造耐火坩埚
C.明矾可用作自来水消毒剂 D.铁粉作食品袋内的脱氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接甲醇燃料电池以其供电量大、持续时间长而极具发展前景,其工作原理如右图。下列关于它的说法正确的是
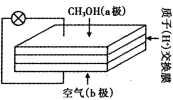
A. 电子自b极经外电路流向a极
B. b极的电极反应式为O2 +4e - +4H+= 2H2O
C. 质子交换膜中的H+流向a极
D. 用该电池电解CuSO4溶液,理论上每生成0.1 molCu消耗氧气1.12 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从镍矿石尾矿中提取NiSO4是解决我国镍资源匮乏的一条重要途径,已知该过程如下:

表1:各物质的Ksp数据如下表:
物质 | MnS | NiS | PbS | CuS | Ni(OH)2 |
Ksp | 2.5×10-13 | 1.1×10-21 | 8.0×10-28 | 6.3×10-36 | 2.0×10-15 |
表2:滤液A中各金属离子的含量如下表:
成分 | Ni2+ | Fe3+ | Fe2+ | Mn2+ | Cu2+ | Pb2+ | …… |
3.80 | 4.80 | x | 0. 20 | 0.15 | <0.001 | …… |
根据以上信息,回答下列问题:
(1)步骤I酸浸之前需将矿石粉碎,目的是____________。
(2)若杂质离子的浓度c≤1.0×10-5mol/L即可认定沉淀完全,则步骤Ⅱ中当Pb2+“恰好沉淀完全时,溶液中硫离子的浓度c(S2-)=_____________
(3)常温下进行步骤Ⅲ的目的是为了除去铁和锰元素,已知除铁元素的离子反应如下:
2Fe2++ ClO - +5H2O=2Fe( OH)3↓+Cl-+4H+
此时Mn2+的氧化产物为MnO2,写出除锰元素的离子方程式______________。
(4)为测定滤液A中Fe2+离子的含量,(每升溶液中含有的亚铁离子的质量,以g/L表示)每次移取20.00 mL待测液,并用0.02 mol/L的KMnO4溶液滴定,若已知其他离子均不反应,且三次滴定平均消耗KMnO4溶液18. 00mL,则x的值为________(精确到小数点后两位)。
(5)所得Ni(OH)2是制造镍镉电池的重要原料,镍镉电池工作原理如下:
Cd+2NiO(OH) +2H2O![]() Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
则随着放电的进行,正极区pH______(填“增大”、“减小”或“不变”);充电时阴极电极反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g) ![]() 2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
A. 生成C的速率与A的消耗的速率相等
B. A、B、C的浓度相等
C. 单位时间生成n mol A,同时生成 2n mol C
D. A、B、C的分子数之比为 1∶3∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com