
| A. | FeCl2 | B. | Fe(OH)3 | C. | NaOH | D. | H2SiO3 |
分析 A.FeCl3和Fe反应生成FeCl2;
B.Fe(OH)2被氧气氧化生成Fe(OH)3;
C.Na2O和水反应生成NaOH;
D.SiO2和水不反应.
解答 解:A.2FeCl3+Fe=3FeCl2,所以可以通过化合反应制取氯化亚铁,故A不选;
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以可以通过化合反应制取氢氧化铁,故B不选;
C.Na2O+H2O=2NaOH,所以可以通过化合反应制取NaOH,故C不选;
D.SiO2和水不反应,所以不能通过化合反应制取硅酸,应该用NaOH溶液制取硅酸钠,然后用硅酸钠和酸反应制取硅酸,故D选;
故选D.
点评 本题考查物质之间的转化,侧重考查元素化合物知识,明确常见物质的性质及常见化学反应是解本题关键,知道硅酸的制取方法,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 2CaO+2S=2CaS+O2↑ | B. | S+O2=SO2 | ||
| C. | CaO+SO2=CaSO3 | D. | 2CaSO3+O2=2CaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧杯 | B. | 漏斗 | C. | 玻璃棒 | D. | 胶头滴管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:3:5 | B. | 2:5:5 | C. | 2:1:5 | D. | 2:2:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鸡蛋清在水中形成的分散系是一种液溶胶,往其中加入饱和(NH4)2SO4溶液会生成白色沉淀 | |
| B. | 可用丁达尔效应来区分胶体和溶液 | |
| C. | 胶体中存在布朗运动,其他分散系中不存在布朗运动 | |
| D. | 某纯净纳米材料其粒子直径从几纳米到几十纳米,该纳米材料属于胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

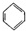 +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$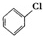 +HCl
+HCl| 项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
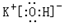 .
.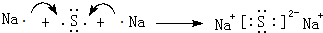 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物. ,该物质是由非极性键(填“极性”或“非极性”)键形成的.
,该物质是由非极性键(填“极性”或“非极性”)键形成的.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | |
| D | E | F |
| A. | D的单质是常见的半导体材料 | |
| B. | B与E形成的化合物不只一种 | |
| C. | C与F的原子序数之差为8 | |
| D. | A的最高价氧化物的水化物能和Al(OH)3反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com