
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1molCu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑CO2的溶解)。则电解过程中共转移电子的物质的量为( )
A. 0.4mol B. 0.5mol C. 0.6mol D. 0.8mol
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源:2016-2017学年河北省石家庄市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A. 向明矾溶液中加入氢氧化钡溶液至沉淀的物质的量达到最大值:Al3++ 2SO42-+ 2Ba2++ 4OH-=2BaSO4↓+ AlO2-+2H2O
B. 向澄清石灰水中通入少量CO2:OH- + CO2=HCO3-
C. 醋酸溶液与水垢中的CaCO3反应:CaCO3 + 2CH3COOH=Ca2++ 2CH3COO-+H2O + CO2↑
D. 硝酸银溶液中加入铜粉:Ag+ + Cu=Cu2+ + Ag
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列名词与环境污染无关的是
A. 酸雨 B. 光化学烟雾 C. 冻雨 D. 水体富营养化
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三上学期期末联考化学试卷(解析版) 题型:选择题
下列有关化学用语的描述不正确的是( )
A. MgF2的电子式: 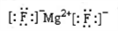
B. 中子数为15的硅原子: 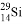
C. 乙烯的结构简式:CH2CH2
D. NH3•H20 的电离方程式: NH3•H20  NH4+ + 0H-
NH4+ + 0H-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二下学期开学考试化学试卷(解析版) 题型:填空题
描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱电解质的电离平衡常数:
酸或碱 | 电离常数(Ka或Kb) | 难(微)溶物 | 溶度积常数(Ksp) |
CH3COOH | 1.8×10-5 | BaSO4 | 1×10-10 |
HNO2 | 4.6×10-4 | BaCO3 | 2.6×10-9 |
HCN | 5×10-10 | CaSO4 | 7×10-5 |
HClO | 3×10-8 | CaCO3 | 5×10-9 |
NH3·H2O | 1.8×10-5 |
请回答下面问题:
(1)上述四种酸中,酸性最弱的是_____________ (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是________________(填序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈________ (选填“酸性”“中性”或“碱性”),理由是__________________,溶液中各离子浓度大小的关系是_____________________。
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大到小排列为_____________________________________。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.0lmol·L-1以上,则溶液中CO32-物质的量浓度应 ≥____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二下学期开学考试化学试卷(解析版) 题型:选择题
电解NaCl溶液的装置如图所示,下列说法不正确的是( )
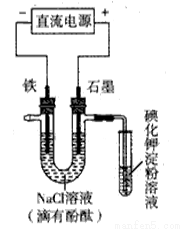
A. 铁电极上的电极反应式为Fe-2e-=Fe2+
B. 溶液中Na+由石墨电极向铁电极移动
C. 通电一段时间后,可看到铁电极附近溶液变红
D. 通电一段时间后,可看到试管中溶液变蓝
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高二上学期期末考试化学试卷(解析版) 题型:简答题
(1)有一种燃料电池,所用燃料为H2和空气,电解质为熔融的K2CO3。回答下列问题
①CO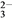 移向____________极。
移向____________极。
②正极反应式为____________________。
③电池中CO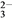 的物质的量将逐渐________________(填增大、减少、不变)。
的物质的量将逐渐________________(填增大、减少、不变)。
(2)用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则
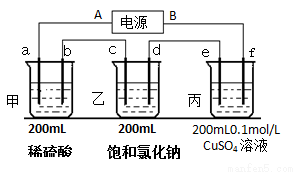
①电源A极是______________极。
②c极上的电极反应式:___________________。
③甲、乙两池共可收集到________mol气体。
④丙装置上某极可析出固体________克,溶液的pH为________________。(常温,不考虑溶液体积变化)
⑤电解n分钟后,硫酸铜正好消耗完,再将e、f电极反接电源,用同样的电流再电解n分钟,则丙溶液中的硫酸铜的物质的量浓度为______________mol/L。(不考虑溶液体积变化)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高二上学期期末考试化学试卷(解析版) 题型:选择题
化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下列是一些化学键的键能,根据键能数据估算反应CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热ΔH为:
化学键 | C﹣H | C﹣F | H﹣F | F﹣F |
键能/(kJ·mol﹣1) | 414 | 489 | 565 | 155 |
A. +485 kJ·mol﹣1 B. ﹣485 kJ·mol﹣1 C. +1940 kJ·mol﹣1 D. ﹣1940 kJ·mol﹣1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试(寒假作业检测)化学试卷(解析版) 题型:选择题
在一定温度下,下列叙述是可逆反应A(g)+3B(g) 2C(g)在定容密闭容器中达到平衡的标志的是
2C(g)在定容密闭容器中达到平衡的标志的是
①C的生成速率与C的分解速率相等;
②单位时间内amol A生成,同时生成3amol B;
③A、B、C的浓度不再变化;
④混合气体的总压强不再变化;
⑤混合气体的平均摩尔质量不再变化;
⑥用A、B、C的物质的量浓度变化表示的反应速率之比为1:3:2;
⑦A、B、C的分子数目比为1:3:2;
⑧混合气体的密度不再变化。
A. ②⑤ B. ①③④⑤ C. ②⑥⑦⑧ D. ⑤⑥⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com