
| A、SO2与紫色石蕊溶液 | B、过量的Cl2与KI淀粉溶液 | C、硫化氢与醋酸铅试纸 | D、Na2O2与酚酞溶液 |


科目:高中化学 来源: 题型:
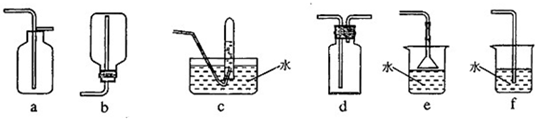
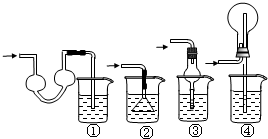 用如图所示装置可以完成一系列实验(图中夹持装置已略去)
用如图所示装置可以完成一系列实验(图中夹持装置已略去)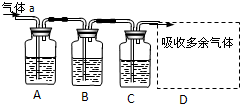
| 装置 | A | B | C | D |
| 试剂 | FeCl2溶液 | 淀粉KI溶液 | 石蕊溶液 | NaOH溶液 NaOH溶液 |
| 现象 | 溶液由浅绿色变为棕黄色 | 溶液变蓝 溶液变蓝 |
先变红后褪色 先变红后褪色 |
|
| 离子方程式 | Cl2+2Fe2+=2Fe3++2Cl- Cl2+2Fe2+=2Fe3++2Cl- |
Cl2+2I-=I2+2Cl- Cl2+2I-=I2+2Cl- |
Cl2+2OH-=Cl-+ClO-+2H2O Cl2+2OH-=Cl-+ClO-+2H2O |
| 装置 | A | B | C |
| 试剂 | 品红溶液 | 酸性高锰酸钾溶液 | 硫化氢的水溶液 |
| 现象 | 红色褪去 红色褪去 |
紫色褪去 | 生成淡黄色沉淀 生成淡黄色沉淀 |
| 体现SO2的性质 | 漂白性 漂白性 |
还原性 还原性 |
氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
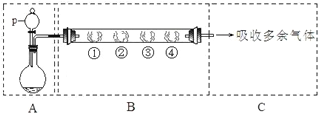
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | 变红 变红 |
褪色 褪色 |
褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | 还原性 还原性 |
氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(2011?山西模拟)下列实验现象、操作或反应原理的解释正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 实验现象 |
| 溶液先变红后褪色 | |
| 有白色沉淀产生 | |
| 有气泡产生,氯水颜色变浅 |
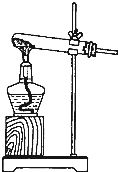
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硫酸滴在润湿的蓝色石蕊试纸上,试纸先变红,然后褪色,最后变黑,说明浓硫酸具有酸性、氧化性和吸水性 | ||||
B、样品
| ||||
| C、常温下浓硫酸能用铁制容器盛装,说明浓硫酸与Fe不反应 | ||||
D、样品
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com