
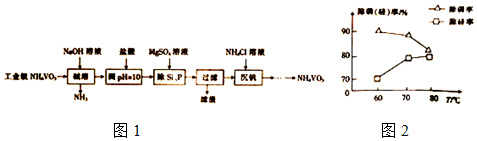
分析 以沉淀法除去工业级偏钒酸铵(NH4VO3)中硅、磷元素杂质的流程为:在偏钒酸铵中加氢氧化钠溶液,将偏钒酸铵溶解,铵盐遇到强碱生成氨气,再加盐酸调节溶液的pH值,加硫酸镁,生成Mg3(PO4)2、MgSiO3沉淀,过滤除去滤渣,在滤液中加氯化铵得偏钒酸铵,
(1)根据气体在水中溶解度的影响因素可知,升温、减压都可以减小气体的溶解度,由于氨气在水中形成氨水能电离出氢氧根离子,根平衡移动原理,增加氢氧根浓度可以减小氨气 的溶解度;
(2)①根据Ksp(MgSiO3)=c(Mg2+)c(SiO32-)=2.4×l0-5,结合c(SiO32-)=0.08mol/L,进行计算;
②根据影响盐类水解的因素可知,升高温度水解程度增大,镁离子、硅酸根离子都是易水解的离子;
(3)沉钒时,反应温度需控制在50℃,可采用水浴加热;
(4)探究NH4Cl的浓度对沉钒率的影响,对比试验应体积形同;
(5)偏钒酸铵与草酸反应生成(NH4)2[(VO)2(C2O4)3]和二氧化碳,据此分析.
解答 解:(1)根据气体在水中溶解度的影响因素可知,升温、减压都可以减小气体的溶解度,故选a,由于氨气在水中形成氨水能电离出氢氧根离子,根平衡移动原理,增加氢氧根浓度可以减小氨气 的溶解度,故选c,
故答案为:ac;
(2)①已知Ksp(MgSiO3)=c(Mg2+)c(SiO32-)=2.4×l0-5,结合c(SiO32-)=0.08mol/L,则c(Mg2+)=$\frac{2.4×1{0}^{-5}}{0.08}mol/L$=3×10-4mol/L,
故答案为:3×10-4mol/L;
②根据影响盐类水解的因素可知,升高温度水解程度增大,镁离子、硅酸根离子都是易水解的离子,所以升温促进Mg2+水解生成Mg(OH)2,使硅酸根水解生成硅沉淀,反应的离子方程式为SiO32-+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$H2SiO3↓+2OH-(或者SiO32-+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$H4SiO4↓+2OH-);
故答案为:升温促进Mg2+水解生成Mg(OH)2;SiO32-+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$H2SiO3↓+2OH-(或者SiO32-+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$H4SiO4↓+2OH-);
(3)沉钒时,反应温度需控制在50℃,可采用水浴加热,
故答案为:水浴加热;
(4)探究NH4Cl的浓度对沉钒率的影响,为要有可比性,两溶液的体积必须相等,所以要 向A中加入约9 mL蒸馏水,使两份溶液总体积相等,便于比较;
故答案为:9;使两份溶液总体积相等,便于比较;
(5)偏钒酸铵与草酸反应生成(NH4)2[(VO)2(C2O4)3],V元素化合价降低,则碳元素化合价升高由二氧化碳生成,则化学方程为:2NH4VO3+4H2C2O4=(NH4)2[(VO)2(C2O4)3]+2CO2↑+4H2O;
故答案为:2NH4VO3+4H2C2O4=(NH4)2[(VO)2(C2O4)3]+2CO2↑+4H2O.
点评 本题考查了物质的制备,涉及对工艺流程的理解、氧化还原反应、对条件的控制选择与理解、溶度积的计算、实验设计等,是对学生综合能力的考查,需要学生具备扎实的基础与灵活运用能力,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,等质量的N2和CO气休的原子数均为2NA | |
| B. | 在反应KC1O4+8HCI=KCl+4Cl2↑+4H2O中,每生成4molCl2转移的电子数为8NA | |
| C. | 含有3mol离子的过氧化钠固体和足量的水反应,电子转移数为NA | |
| D. | 标准状况下,80gSO3中含3NA个氧原子,体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol 硫酸钾中阴离子所带电荷数为NA | |
| B. | 将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NAFe3+ | |
| C. | 乙烯和环丙烷(C3H6)组成的28g混合气体中含有3NA个氢原子 | |
| D. | 标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁与醋酸:Fe2O3+6H+═2Fe3++3H2O | |
| B. | 碳酸钠与盐酸:Na2CO3+2H+═2Na++CO2↑+H2O | |
| C. | 铁片插入到硫酸铜溶液中:2Fe+3Cu2+═2Fe3++3Cu | |
| D. | 向盐酸中加入适量氨水:H++NH3•H2O═NH4++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的A、B两种烃分别完全燃烧后,生成的CO2与消耗的O2的物质的量均相同,则A和B一定互为同系物 | |
| B. | 沸点比较:正戊烷>异戊烷>新戊烷 | |
| C. | 乙酸与乙醇在一定条件下反应生成乙酸乙酯和水的反应属于取代反应 | |
| D. | 判断苯分子中不存在碳碳单键与碳碳双键的交替结构的依据是:邻二甲苯只有一种结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 )的一条路线如图:
)的一条路线如图: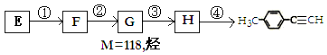
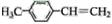 .
. 、
、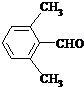 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CO18OC2H5+H2O $?_{△}^{稀硫酸}$ CH3COOH和C2H518OH | |
| B. | 溴乙烷与氢氧化溶液共热:CH3CH2Br+NaOH $→_{△}^{水}$ CH3CH2OH+NaBr | |
| C. | 蔗糖水解: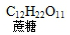 +H2O$\stackrel{催化剂}{→}$ +H2O$\stackrel{催化剂}{→}$ | |
| D. | 苯酚钠中通入二氧化碳: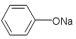 +CO2+H2O→ +CO2+H2O→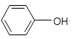 +NaHCO3 +NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
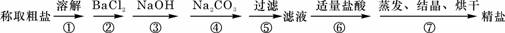
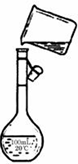 (5)为检验精盐纯度,需配制100mL 1mol/L NaCl溶液,右图是该同学转移溶液的示意图,图中的错误是未用玻璃棒引流
(5)为检验精盐纯度,需配制100mL 1mol/L NaCl溶液,右图是该同学转移溶液的示意图,图中的错误是未用玻璃棒引流查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com