
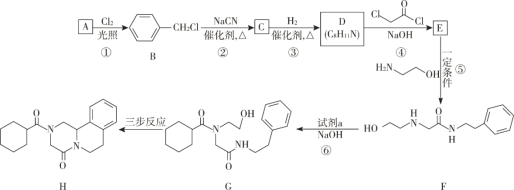
【题目】吡喹酮(H)是一种治疗血吸虫病的药物,合成路线如下图所示:
已知:I R-Cl+NaCN![]() R-CN+NaCl
R-CN+NaCl
ii 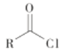 +R′-NH-R"+NaOH
+R′-NH-R"+NaOH![]()
 +NaCl+H2O(R、R′表示烃基,R"表示烃基或H)
+NaCl+H2O(R、R′表示烃基,R"表示烃基或H)
(1)A 属于芳香烃,其名称是________________________。
(2)步骤②的反应类型是_______________________________。
(3)B 的一种同分异构体,含苯环且核磁共振氢谱中出现三组峰,其结构简式为______________。
(4)③中 1mol C 理论上需要消耗__________________mol H2生成 D。
(5)④的化学方程式是 ________。
(6)F 中含氧官能团是 ![]() 和_______________________(填名称)。
和_______________________(填名称)。
(7)试剂 a 的结构简式是___________________。
(8)G→H 分为三步反应,J 中含有 3 个六元环,写出 I、J 的结构简式。
![]()
I:_____;J:_____。
【答案】甲苯 取代反应 ![]() 2
2 ![]() +
+![]() +NaOH→
+NaOH→![]() +NaCl+H2O 羟基
+NaCl+H2O 羟基 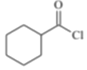

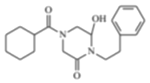
【解析】
A属于芳香烃,说明含有苯环,A发生取代反应生成B,由B可知A为![]() ,B发生信息i的反应生成C,C为
,B发生信息i的反应生成C,C为![]() ,C发生还原反应生成D,根据D分子式知,D为
,C发生还原反应生成D,根据D分子式知,D为![]() ,D发生信息ii的反应生成E,E发生取代反应生成F,根据F的结构简式知,E为
,D发生信息ii的反应生成E,E发生取代反应生成F,根据F的结构简式知,E为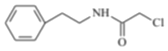 ,F发生取代反应生成G,根据F、G的结构简式及信息ii知,a为
,F发生取代反应生成G,根据F、G的结构简式及信息ii知,a为 ,据此分析解答。
,据此分析解答。
(1)A为![]() ,名称为甲苯,故答案为:甲苯;
,名称为甲苯,故答案为:甲苯;
(2)步骤②发生信息i的反应生成C,属于取代反应,故答案为:取代反应;
(3)B(![]() )的一种同分异构体,含苯环且核磁共振氢谱中出现三组峰,其结构简式为
)的一种同分异构体,含苯环且核磁共振氢谱中出现三组峰,其结构简式为![]() ,故答案为:
,故答案为:![]() ;
;
(4)C为![]() ,D为
,D为![]() ,即C中-C≡N转化为-CH2NH2,③中1molC理论上需要消耗2molH2生成D,故答案为:2;
,即C中-C≡N转化为-CH2NH2,③中1molC理论上需要消耗2molH2生成D,故答案为:2;
(5)④发生信息ii的反应生成E,反应的化学方程式为![]() +
+![]() +NaOH→
+NaOH→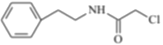 +NaCl+H2O,故答案为:
+NaCl+H2O,故答案为:![]() +
+![]() +NaOH→
+NaOH→![]() +NaCl+H2O;
+NaCl+H2O;
(6)F(![]() )中的含氧官能团是
)中的含氧官能团是 和羟基,故答案为:羟基;
和羟基,故答案为:羟基;
(7)根据上述分析,试剂a的结构简式为 ,故答案为:
,故答案为: ;
;
(8)G→H 分为三步反应,G(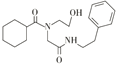 )先发生催化氧化生成I,I结构简式为
)先发生催化氧化生成I,I结构简式为 ,I发生加成反应生成J,J中含有3个六元环,则J为
,I发生加成反应生成J,J中含有3个六元环,则J为 ,最后J分子内脱水生成H(
,最后J分子内脱水生成H(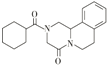 ),故答案为:
),故答案为: ;
; 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】王浆酸是从蜂王浆中分离出的一种有机酸,它有很好的杀菌、抗癌、抗放射及强化机体、增强免疫力的作用,其结构如下所示。有关王浆酸的说法不正确的是( )
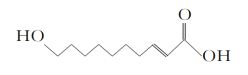
A. 分子式为C10H18O3
B. 能使溴的四氯化碳溶液褪色
C. 一定条件下能发生取代反应和氧化反应
D. 1 mol王浆酸最多能中和2 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )

A. 上下移动①中铜丝可控制SO2的量
B. ②中选用品红溶液验证SO2的生成
C. ③中选用NaOH溶液吸收多余的SO2
D. 为确认CuSO4生成,向①中加水,观察颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇结构式如图所示,“箭头”表示乙醇发生化学反应时分子中可能断键的位置,下列叙述中不正确的是( )
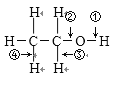
A. 与钠反应时断裂①键B. 发生消去反应时断裂②④键
C. 与乙酸发生酯化反应时断裂②键D. 发生催化氧化反应时断裂①③键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是重要的金属,广泛应用于电气、机械制造、国防等领域,铜的化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1)CuSO4晶体中S原子的杂化方式为________,SO42-的立体构型为_______________。
(2)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
![]()
①NH4CuSO3中金属阳离子的核外电子排布式为__________________。N、O、S三种元素的第一电离能大小顺序为__________________________(填元素符号)。
②向CuSO4溶液中加入过量氨水,可生成[Cu(NH3)4]SO4,下列说法正确的是________
A.氨气极易溶于水,原因之一是NH3分子和H2O分子之间形成氢键的缘故
B.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
C.Cu(NH3)4]SO4溶液中加入乙醇,会析出深蓝色的晶体
D.已知3.4 g氨气在氧气中完全燃烧生成无污染的气体,并放出a kJ热量,则NH3的燃烧热的热化学方程式为:NH3(g)+3/4O2(g)=1/2N2(g)+3/2H2O(g) ΔH=-5a kJ·mol-1
(3)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如下左图所示。


①1 mol氨基乙酸钠(H2NCH2COONa)含有σ键的数目为________________。
②氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:____________(写化学式)。
③已知:硫酸铜灼烧可以生成一种红色晶体,其结构如上右图所示。则该化合物的化学式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)烃A在同温、同压下蒸气的密度是H2的35倍,其分子式为________。
(2)3—甲基—1一丁炔的结构简式为________
(3)![]() 的分子式为__________
的分子式为__________
(4)分子式为C8H10属于芳香烃的同分异构体共有______种,其中_______(结构简式)在苯环上的一氯取代产物有两种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,莽草酸的结构简式如图所示。下列关于莽草酸的说法正确的是( )
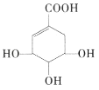
A.分子式为![]() B.分子中含有2种官能团
B.分子中含有2种官能团
C.可发生加成反应和取代反应D.1mol莽草酸与足量的Na反应,标况下生成33.6LH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是一个远未完全开发的巨大化学资源宝库。
(1)无需经过化学变化就能从海水中获得的物质是________(填序号)
A 氯气 B 淡水 C烧碱 D 食盐
(2)从海水制得的粗盐中含有较多的Mg2+、Ca2+、SO![]() 等,要除去这些离子,下列加入药品顺序正确的是________(填序号)
等,要除去这些离子,下列加入药品顺序正确的是________(填序号)
A NaOH溶液→Na2CO3溶液→BaCl2溶液B BaCl2溶液→NaOH溶液→Na2CO3溶液
C NaOH溶液→BaCl2溶液→Na2CO3溶液D Na2CO3溶液 →NaOH溶液→ BaCl2溶液
(3)从海水中得到溴的过程如下:
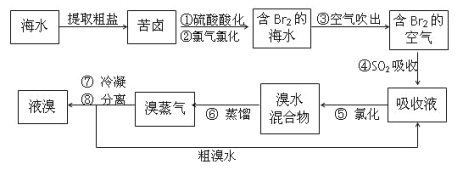
①写出由“苦卤”变成“含溴海水”的离子方程式________
②写出④发生反应的化学方程式________
③某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图所示实验装置:
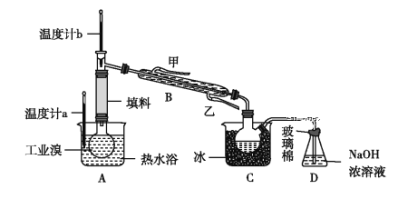
图中仪器B冷却水的出口为______(填“甲”或“乙”),D装置的作用是__________,反应的离子方程式为__________,整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
(4)已知某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,现欲使溶液中的Cl-、Br-、I-的物质的量之比为变为4:3:2,那么通入Cl2的物质的量是原溶液中I-的物质的量的__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各选项能说明分子式为C4H6的烃是HC![]() C-CH2-CH3,而不是CH2=CH-CH=CH2的事实是( )
C-CH2-CH3,而不是CH2=CH-CH=CH2的事实是( )
A. 燃烧时有黑烟
B. 能使KMnO4酸性溶液褪色
C. 所有原子都在同一平面上
D. 与足量溴水反应,生成物中只有2个碳原子上有溴原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com