
已知34Se、35Br位于同一周期,下列关系正确的是
A.热稳定性:HCl>H2Se>HBr B.还原性:Se2->S2->Cl-
C.原子半径:Se>Cl>P D.酸性:H2SeO4>H2SO4>H3PO4
科目:高中化学 来源: 题型:
H2C=CHOH不稳定,在常温下为液体,很容易转化成稳定的CH3CHO。然而,2002年的美国《科学》杂志报道:外太空的某一个星球的大气层含有大量的H2C=CHOH。请预测该星球的温度是
A.较低温度 B.较高温度
C.无法判断温度的高低 D.上述说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO(g)+H2O(g)  CO2(g)+H2(g) ∆H=– 41 kJ/mol
CO2(g)+H2(g) ∆H=– 41 kJ/mol
相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。
相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系 能量的变化 | ||||
| CO | H2O | CO2 | H2 | |||
| ① | 1 | 4 | 0 | 0 | 放出热量:32.8 kJ |
|
| ② | 0 | 0 | 1 | 4 | 热量变化:Q |
|
下列说法中,不正确的是
A.容器①中反应达平衡时,CO的转化率为80%
B.容器①中CO的转化率等于容器②中CO2的转化率
C.平衡时,两容器中CO2的浓度相等
D.容器①中反应速率:v(CO)= v(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
同周期主族元素,随原子序数递增,下列说法中错误的是
A.最外层电子数逐渐增多 B.元素最高正化合价均由+1递增到+7
C.原子半径逐渐减小 D.金属性逐渐减弱,非金属性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
湖南省常德市石门县鹤山村用土法炼砒霜导致地下水砷污染严重,157人中毒死亡。关于砷(33As)的说法不正确的是
A.砷的氢化物和磷的氢化物的稳定性为PH3<AsH3
B.砷原子核内有33个质子
C.砷是第四周期第VA族
D.砷的最高价氧化物对应的水化物的化学式是H3AsO4
查看答案和解析>>
科目:高中化学 来源: 题型:
加强空气质量检测,客观分析空气中污染物的来源及性质,将有助于制定有针对性的治理措施。下表是某城市某日的空气质量报告:
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | SO2 | II | 良 |
该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行了如下探究:
(1)用下图所示装置进行实验。
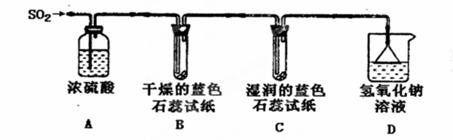
①A装置的作用是____________________。
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊
试纸变成________________色,说明SO2与水反应生成一种酸,其化学反应方程式是 。
③D装置的作用是__________________________________________________,
D中发生反应的化学方程式是_________________________________________。
(2)往盛有水的烧杯中通入SO2气体,测得所得溶液的pH________7(填“>”“=”或“<”),然后每隔1h测定其pH,发现pH逐渐_______(填“变大”或“变小”), 直至恒定,原因是 (写出反应的离子方程式)。
(3)SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4, 则在此过程中的飘尘是作为___________(填“催化剂”或“氧化剂”)。
(4)SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
(5)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为__________________,是造成酸雨的另一主要原因。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.CO2、BF3、PCl3分子中所有原子的最外层电子都满足8电子稳定结构
B.P4和CH4都是正四面体分子且键角都为109o28ˊ
C.乙烯分子有5个σ键,1个π键
D.丙烯分子中3个碳原子都是sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
水能与多种金属离子形成络合物,某红紫色络合物的组成为CoCl3·5NH3·H2O。其水溶液显弱酸性,加入强碱加热至沸腾有氨放出,同时产生Co2O3沉淀;加AgNO3于该化合物溶液中,有AgCl沉淀生成,过滤后加AgNO3溶液于滤液中无变化,但加热至沸腾有AgCl沉淀生成, 且其质量为第一次沉淀量的二分之一。则该配合物的化学式最可能为( )
A.[ CoCl2(NH3)4 ]Cl·NH3·H2O B.[ Co(NH3)5(H2O)]Cl3
C.[ CoCl2(NH3)3(H2O)]Cl·2NH3 D.[ CoCl(NH3)5]Cl2·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐和工业用盐具有广泛的用途。已知工业用盐主要成分为NaNO2,外观酷似食盐并有咸味。NaNO2有氧化性和还原性,遇酸分解放出NO2。
(1)下列试剂可鉴别工业用盐和食盐的是________。
a.H2O b.硝酸酸化的硝酸银
c.盐酸
(2)NaNO2与氢碘酸反应(含氮产物为NO)的离子方程式为______________。
(3)某工厂废液中含有2%~5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2中的氮转化为对空气无污染的气体,该物质是________。
a.NaCl b.NH4Cl c.浓H2SO4
(4)氯碱工业通过电解饱和食盐水来获得相应的产物。请写出电解食盐水的离子方程式______________________________________,
若在标准状况下生成3.36 L H2,则溶液中生成的OH-的物质的量为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com