
化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下列相关说法正确的是________(填序号)。
A.通过某种电池单位质量或单位体积所能输出能量的多少,可以判断该电池
的优劣
B.二次电池又称充电电池或蓄电池,这类电池可无限次重复使用
C.除氢气外,甲醇、汽油、氧气等都可用作燃料电池的燃料
D.近年来,废电池必须进行集中处理的问题被提上日程,其首要原因是电池外壳的金属材料需要回收
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应式可表示为
2Ni(OH)2+Cd(OH)2 Cd+2NiO(OH)+2H2O
Cd+2NiO(OH)+2H2O
已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法正确的是________(填序号)。
A.以上反应是可逆反应
B.反应环境为碱性
C.电池放电时Cd作负极
D.该电池是一种二次电池
(3)在宇宙飞船和其他航天器上经常使用的氢氧燃料电池是一种新型电源,其构造如图所示:a、b两个电极均由多孔的碳块组成,通入的氢气和氧气由孔隙中逸入,并在电极表面发生反应而放电。
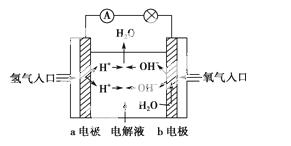
①a电极是电源的________极;
②若该电池为飞行员提供了360 kg的水,则电路中通过
了________mol电子。
(4)请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱,请画出实验装置图并写出电极反应式。
科目:高中化学 来源: 题型:
)A至I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为地壳中含量最多的金属元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元 素。
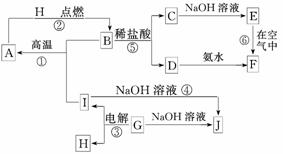
请填写下列空白:
(1) 写出下列物质的化学式:A______________,G_____________, B ;
(2) 若C→D为化合反应,则此时的化学方程式为:
_________________________ ______;
(3) 写出E→F的化学方程式:
________________________________________________________________________;
(4) 写出反应④的离子方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以甲烷燃料电池为例来分析在不同的环境下电极反应式的书写方法:
(1)酸性条件
燃料电池总反应式:CH4+2O2 ===CO2+
===CO2+ 2H2O①
2H2O①
燃料电池正极反应式:O2+4H++4e-===2H2O②
①-②×2,得燃料电池负极反应式:__________________________。
(2)碱性条件
燃料电池总反应式:CH4+2O2+2NaOH===Na2CO3+3H2O①
燃料电池正极反应式:O2+2H2O+4e-===4OH-②
①-②×2,得燃料电池负极反应式:_________________________。
(3)固体电解质(高温下能传导O2-)
燃料电池总反应式:CH4+2O2===CO2+2H2O①
燃料电池正极反应式:O2+4e-===2O2-②
①-②×2,得燃料电池负极反应式:_____________________________。
(4)熔融碳酸盐(如:熔融K2CO3)环境下电池总反应式:CH4+2O2===CO2+2H2O。正极电极反应式:O2+2CO2+4e-===2CO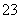 。电池总反应式-正极电极反应式得负极电极反应式:________________________。
。电池总反应式-正极电极反应式得负极电极反应式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
银制器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的的银器浸入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是( )
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al + 3Ag2S = 6Ag + Al2S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使 其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是( )。
其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是( )。

A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
D.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
查看答案和解析>>
科目:高中化学 来源: 题型:
比较下列反应或过程中的热量或反应热的相对大小。
(1)已知:①H2(g)+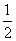 O2(g)===H2O(g)
O2(g)===H2O(g)
ΔH1=a kJ·mol-1
②2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1
③H2(g)+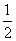 O2(g)===H2O(l) ΔH3=c kJ·mol-1
O2(g)===H2O(l) ΔH3=c kJ·mol-1
④2H2(g)+O2(g)===2H2O(l) ΔH4=d kJ·mol-1
则a、b、c、d间的大小关系为____________________________________________。
(2)若向三份等体积0.100 0 mol·L-1 NaOH溶液中分别加入①稀醋酸,②浓H2SO4,③稀硝酸至恰好完全反应,则上述过程中的焓变ΔH1、ΔH2、ΔH3的大小关系为________________________________________________。
(3)已知胆矾溶于水时,溶液温度降低。在室温下将1 mol无水硫酸铜制成溶液时,放出热量为Q1 kJ,而胆矾分解的热化学方程式是CuSO4·5H2O(s)===CuSO4(s)+5H2O(l) ΔH=+Q2 kJ·mol-1,则Q1与Q2的大小关系为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应过程能量变化如图所示,下列说法正确的是

A、反应过程a有催化剂参与
B、该反应为放热反应,热效应等于△H
C、改变催化剂,可改变该反应的活化能
D、有催化剂的条件下,反应的活化能等于E1+E2
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)是火箭发动机的燃料,它与N2O4反应时,N2O4为氧化剂,生成氮气和水蒸气。已知:N2(g)+2O2(g)===N2O4(g) ΔH=+8.7 kJ/mol,N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534.0 kJ/mol,下列表示肼跟N2O4反应的热化学方程式,正确的是( )
A.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-542.7 kJ/mol
B.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-1 059.3 kJ/mol
C.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-1 076.7 kJ/mol
D.N2H4(g)+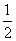 N2O4(g)===
N2O4(g)===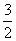 N2(g)+2H2O(
N2(g)+2H2O( g) ΔH=-1 076.7 kJ/mol
g) ΔH=-1 076.7 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物Ⅴ是中药黄芩中的主要活性成分之一,具有抗氧化和抗肿瘤作用。化合物Ⅴ也可通过下图所示方法合成:

回答下列问题:
(1)化合物Ⅲ的分子式为 ,1 mol该物质完全燃烧需消耗 mol O2.
(2)化合物Ⅱ的合成方法为:
|
 -CHO+(CH3CO)2O →
-CHO+(CH3CO)2O →
 -CH=CHCOOH+ A
-CH=CHCOOH+ A
 |
|

 -CH=CHCOOH 化合物Ⅱ
-CH=CHCOOH 化合物Ⅱ 已知在合成肉桂酸的化学反应中,反应物的物质的量之比为1︰1,生成物A可与饱和NaHCO3溶液反应产生气体,则生成物A的结构简式是 。
(3)反应①的反应类型为 。化合物Ⅰ和Ⅱ反应还可以得到一种酯,生成该酯的反应方程式为 。(不用注明反应条件)
(4)下列关于化合物Ⅳ、Ⅴ的说法正确的是 (填序号)。
a.都属于芳香化合物
b.都能与H2发生加成反应,Ⅳ消耗的H2更多
c.都能使酸性KMnO4溶液褪色
d.都能与FeCl3溶液发生显色反应
(5)满足以下条件的化合物Ⅰ的同分异构体Ⅵ的结构简式为
①遇FeCl3溶液显示紫色
②l mol Ⅵ与浓溴水反应,最多消耗1 mol Br2
③Ⅵ的核磁共振氢谱有五组峰,峰面积之比为1︰1︰2︰2︰6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com