
²æ·Ö½šŹōæÉŅŌÓėĖ®ŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦”£
£Ø1£©½«Ņ»Š”æ齚ŹōÄĘĶ¶ČėŹ¢ÓŠĖ®µÄÉÕ±ÖŠ£¬“żĶźČ«·“Ó¦ŗó£¬ĻņĘäÖŠµĪ¼Ó·ÓĢŖČÜŅŗ”£¢ŁÄĘÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ ”£
¢ŚÉĻŹöŹµŃé¹ż³ĢÖŠ£¬æɹŪ²ģµ½µÄŹµŃéĻÖĻóÓŠ £ØĢīŃ”ĻīŠņŗÅ£©£¬
²śÉśĻÖĻóbµÄŌŅņŹĒ ”£
a£®ÄĘø”ŌŚĖ®Ćę b£®ÄĘČŪ³ÉŠ”Ēņ
c£®ÄĘĒņŌŚĖ®ĆęÉĻĖÄ“¦ÓĪ¶Æ£¬·¢³öĖ»Ė»Éł£¬Öš½„ĻūŹ§
d£®·“Ó¦ŗóĻņÉÕ±ÖŠµĪ¼Ó·ÓĢŖČÜŅŗ£¬ČÜŅŗ³ŹŗģÉ«
£Ø2£©Ģś·ŪæÉŅŌÓėĖ®ÕōĘųŌŚøßĪĀĻĀ·“Ó¦£¬Éś³É £ØĢī»ÆѧŹ½£©ŗĶĒāĘų”£
£Ø1£©¢Ł2Na + 2H2O == 2NaOH + H2”ü ¢Śa b c d ·“Ó¦·Å³ö“óĮæµÄČČ£¬ÄʵÄČŪµć½ĻµĶ£Ø2£©Fe3O4
½āĪöŹŌĢā·ÖĪö£ŗ£Ø1£©ÄĘÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ¢Ł2Na + 2H2O == 2NaOH + H2”ü”£¢ŚÓÉÓŚNaµÄĆܶȱČĖ®Š”£¬ĖłŅŌø”ŌŚĖ®ĆęÉĻ£»ÓÉÓŚNaµÄČŪµćµĶ£¬NaÓėĖ®µÄ·“Ó¦ÓÖŹĒ·ÅČČ·“Ó¦£¬·“Ó¦·Å³öµÄČČŹĒNaČŪ»Æ£¬ĖłŅŌÄĘČŪ³ÉŠ”Ēņ£»NaÓėĖ®·“Ó¦²śÉśĒāĘų£¬ĒāĘųÅŻĘĘĮŃ²śÉśĖ»Ė»Éł£¬ÓÉÓŚNaĒņŹÜµ½µÄø÷øö·½ĻņµÄĮ¦“󊔲»µČ£¬ĖłŅŌŌŚĖ®ĆęÉĻĖÄ“¦ÓĪ¶Æ£» NaÓėĖ®·“Ó¦²śÉśNaOH£¬Ź¹ČÜŅŗĻŌ¼īŠŌ£¬µĪ¼Ó·ÓĢŖŹŌ¼Į£¬ČÜŅŗ±äĪŖŗģÉ«”££Ø2£©Ģś·ŪæÉŅŌÓėĖ®ÕōĘųŌŚøßĪĀĻĀ·“Ó¦£¬·½³ĢŹ½ĪŖ3Fe+4H2O(g)  Fe3O4+4H2”ü”£æɼū·“Ó¦²śĪļÓŠFe3O4ŗĶĒāĘų”£
Fe3O4+4H2”ü”£æɼū·“Ó¦²śĪļÓŠFe3O4ŗĶĒāĘų”£
æ¼µć£ŗ漲齚ŹōNa”¢FeÓėĖ®·“Ó¦µÄĢõ¼ž”¢ĻÖĻó¼°·“Ó¦²śĪļ”¢·½³ĢŹ½µÄŹéŠ“µÄÖŖŹ¶”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ½šŹōµ„ÖŹÖŠ£¬²»ÄÜ“ÓČÜŅŗÖŠÖĆ»»³öĶµÄŹĒ£Ø £©
| A£®Zn | B£®Al | C£®Na | D£®Fe |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
2003ÄźÅµ±“¶ū»Æѧ½±ŹŚÓčĮĖĆĄ¹śæĘѧ¼ŅPeter AgreŗĶRoderick MackinnonŅŌ±ķÕĆĖūĆĒŌŚ”°Ė®ĶصĄ”±ŗĶ”°Ąė×ÓĶصĄ”±µÄŃŠ¾æ³É¾Ķ”£Mackinnon½ĢŹŚµÄŃŠ¾æÄŚČŻÖ÷ŅŖŹĒNa+”¢K+Ģå»żŗܽӽü£¬µ«ŌŚÉśĪļĢåÄŚ³ŹĻֵIJī±šČ“øß“ļ1Ķņ±¶£¬ĖūøļĆüŠŌµÄČĆæĘѧ¼Ņ¹Ū²āNa+”¢K+ŌŚ½ųČėĄė×ÓĶصĄĒ°”¢ĶصĄÖŠŅŌ¼°“©¹żĶصĄŗóµÄדĢ¬£¬æÉĪŖ²”ČĖŌŚ”°Ąė×ÓĶصĄ”±ÖŠŃ°ÕŅ¾ßĢåµÄ²”Ņņ£¬²¢ŃŠÖĘĻąÓ¦Ņ©Īļ”£ĻĀĮŠ¹ŲÓŚÄĘ”¢¼ŲµÄĖµ·ØÕżČ·µÄŹĒ
| A£®µ„ÖŹÄʵÄĆÜ¶Č±Č¼ŲµÄĆܶȊ” |
| B£®Na+ŗĶK+³£ÓĆ×÷Ńõ»Æ¼Į |
| C£®ÄĘŗĶ¼Ų¶¼ŹĒ¶ĢÖÜĘŚŌŖĖŲ |
| D£®ÄĘŗĶ¼ŲµÄŗĻ½š[¦Ų(K)=50%~80%]ŌŚŹŅĪĀĻĀ³ŹŅŗĢ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
½«Cuʬ·ÅČė0£®1 mol£ÆL FeCl3ČÜŅŗÖŠ£¬·“Ó¦Ņ»¶ØŹ±¼äŗóČ”³öCuʬ£¬ČÜŅŗÖŠC£ØFe3+£©£ŗC£ØFe2+£©=2£ŗ3£¬ŌņCu2+ÓėFe3+µÄĪļÖŹµÄĮæÖ®±ČĪŖ £Ø £©
| A£®3£ŗ2 | B£®3£ŗ5 | C£®4£ŗ3 | D£®3£ŗ4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
¹¤ŅµÉĻ±ŗÉÕĆ÷·Æ[ KAl(SO4)2”¤12H2O]µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
4 KAl(SO4)2”¤12H2O+3S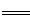 2K2SO4+2Al2O3 +9SO2 +48H2O£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
2K2SO4+2Al2O3 +9SO2 +48H2O£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
| A£®ŌŚ±ŗÉÕĆ÷·ÆµÄ·“Ó¦ÖŠ£¬»¹Ō¼ĮÓėŃõ»Æ¼ĮµÄĪļÖŹµÄĮæÖ®±ČŹĒ3£ŗ4 |
| B£®×īŗóµĆµ½µÄK2SO4ČÜŅŗ³ŹÖŠŠŌ£¬ĖłŅŌc(K+)=c(SO42-) |
| C£®±ŗÉÕ²śÉśµÄSO2æÉÓĆÓŚÖĘĮņĖį,±ŗÉÕ948 tĆ÷·Æ(M=" 474" g/mol)£¬ČōSO2µÄĄūÓĆĀŹĪŖ96%£¬æÉÉś²śÖŹĮæ·ÖŹżĪŖ98%µÄĮņĖį432 t |
| D£®¹¤ŅµÉĻŅ±Į¶Al2O3ÖʵĆAl£¬ŅŌAlŗĶNiO(OH)ĪŖµē¼«£¬NaOHČÜŅŗĪŖµē½āŅŗ×é³ÉŅ»ÖÖŠĀŠĶµē³Ų£¬·ÅµēŹ±NiO(OH)×Ŗ»ÆĪŖNi(OH)2£¬øƵē³Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ |
 NaAlO2£«3Ni(OH)2
NaAlO2£«3Ni(OH)2²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
Č”Ņ»Š”æéÄĘ£¬ÓĆĀĖÖ½Č„µōĆŗÓĶ£¬·ÅŌŚŹÆĆŽĶųÉĻ¼ÓČČ£¬ĻĀĮŠŹµŃéĻÖĻóµÄĆčŹöÕżČ·µÄŹĒ ¢Ł½šŹōÄĘĻČČŪ»Æ ¢ŚŌŚæÕĘųÖŠČ¼ÉÕ³Ź²Ō°×É«»šŃęĒŅ»š»ØĖĽ¦ ¢ŪČ¼ÉÕŗóµĆµ½°×É«¹ĢĢå ¢ÜČ¼ÉÕŹ±ÓŠ»ĘÉ«»šŃę ¢ŻČ¼ÉÕŗóÉś³Éµ»ĘÉ«¹ĢĢå
| A£®¢Ł¢Ś¢Ż | B£®¢Ł¢Ü¢Ż | C£®¢Ł¢Ś¢Ū | D£®¢Ł¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠø÷Ķ¼Óė±ķŹöŅ»ÖĀµÄŹĒ
| A£®Ķ¼¢ŁæÉŅŌ±ķŹ¾¶Ōij»ÆŃ§Ę½ŗāĢåĻµøıäĪĀ¶Čŗó·“Ó¦ĖŁĀŹĖꏱ¼äµÄ±ä»Æ |
| B£®Ķ¼¢ŚbĒśĻß±ķŹ¾·“Ó¦CH2=CH2£Øg£©+H2£Øg£©”śCH3£CH3£Øg£©¦¤H <0£¬Ź¹ÓĆ“ß»Æ¼ĮŹ±£¬·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ |
| C£®ĒśĻßĶ¼¢ŪæÉŅŌ±ķŹ¾ĻņŅ»¶ØĮæµÄĒāŃõ»ÆÄĘČÜŅŗÖŠµĪ¼ÓŅ»¶ØÅضČĀČ»ÆĀĮČÜŅŗŹ±²śÉś³ĮµķµÄĪļÖŹµÄĮæ±ä»Æ |
| D£®Ķ¼¢Üµē½ā±„ŗĶŹ³ŃĪĖ®µÄ×°ÖĆÖŠŅõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ2H++ 2e- = H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠø÷×éĪļÖŹĻą»„·“Ó¦ŗó,ŌŁĻņµĆµ½µÄČÜŅŗÖŠµĪČėKSCNŹŌ¼Į,ČÜŅŗ±ä³ÉŗģÉ«µÄŹĒ
| A£®ĀČĖ®ŗĶĀČ»ÆŃĒĢśČÜŅŗ | B£®ĢśŠ¼ŗĶĀČ»ÆĶČÜŅŗ |
| C£®ĢśŠ¼ŗĶ¹żĮæĻ”ĮņĖį | D£®¹żĮæĢśŠ¼ŗĶĀČ»ÆĢśČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
1 Lij»ģŗĻČÜŅŗÖŠ£¬ČÜÖŹX”¢YÅØ¶Č¶¼ĪŖ0.1mol”¤L”Ŗ1£¬Ļņ»ģŗĻČÜŅŗÖŠµĪ¼Ó0.1 mol”¤L”Ŗ1ijČÜŅŗZ£¬ĖłµĆ³ĮµķµÄĪļÖŹµÄĮæČēĶ¼ĖłŹ¾£¬ŌņX”¢Y”¢Z·Ö±šŹĒ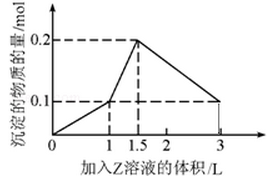
| A£®ĀČ»ÆĀĮ”¢ĀČ»ÆĆ¾”¢ĒāŃõ»ÆÄĘ |
| B£®Ę«ĀĮĖįÄĘ”¢ĒāŃõ»Æ±µ”¢ĮņĖį |
| C£®ĀČ»ÆĀĮ”¢ĀČ»ÆĢś”¢ĒāŃõ»ÆÄĘ |
| D£®Ę«ĀĮĖįÄĘ”¢ĀČ»Æ±µ”¢ĮņĖį |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com