
下列关于电离平衡常数(K)的说法正确的是
A.不同浓度的同一弱电解质,其电离平衡常数(K)不同
B.电离平衡常数(K)越小,表示弱电解质电离能力越弱
C.多元弱酸各步电离平衡常数相互关系为:K1<K2<K3
D.CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小
科目:高中化学 来源: 题型:
在a L的密闭容器里,于一定温度下进行2A(g)+B(g)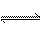 2C(g)的可逆反应。容器内开始加入下列各组物质,在达到平衡时逆反应速率最大的一组物质是( )]
2C(g)的可逆反应。容器内开始加入下列各组物质,在达到平衡时逆反应速率最大的一组物质是( )]
A.2 mol A和1 mol B B.1 mol A和1 mol B
C.1 mol A和2 mol B D.1 mol B和1 mol C
查看答案和解析>>
科目:高中化学 来源: 题型:
在稀氨水中存在平衡:NH3+H2O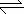 NH
NH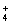 +OH-,如进行下列操作,则NH3、NH
+OH-,如进行下列操作,则NH3、NH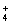 、H+、OH-浓度如何变化?请用“增大”“减小”“不变”填写。
、H+、OH-浓度如何变化?请用“增大”“减小”“不变”填写。
(1)通适量HCl气体时,c (NH3) ,c (H+) 。
(2)加入少量NaOH固体时,c(NH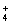 ) ,c (OH-) 。
) ,c (OH-) 。
(3)加入NH4Cl晶体时,c (NH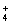 ) ,c (OH-) 。
) ,c (OH-) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学反应速率的认识正确的是
A.H+和OH—的反应活化能接近于零,反应几乎在瞬间完成
B.对于任何化学反应来说,反应速率越大,反应现象就越明显
C.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大
D.化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,将一定量的冰醋酸(无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示。
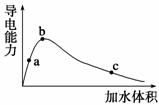
请完成下列问题:
(1)上述a、b、c三点对应醋酸的电离程度最大的是 (填“a”、“b”、“c”),三点对应溶液中c(OH-)由大到小的顺序为 。
(2)c点对应的溶液中c(H+)与c(CH3COO-)+c(OH-)的关系为前者 (填“大于”“小于”“等于”)后者。
(3)从a点到b点,溶液中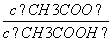 的比值 (填“增大”、“减小”、“等于”)。
的比值 (填“增大”、“减小”、“等于”)。
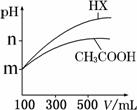
(4)25 ℃时,体积均为100 mL 、pH=m的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示。则稀释前两溶液中c(OH-)= , HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(5)若用pH试纸进行实验,你能否区分上述HX和CH3COOH两种酸溶液?若能,请简述操作过程;若不能,请说明理由。 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学平衡移动的分析中,不正确的是( )
①已达平衡的反应C(s)+H2O(g)⇌CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g)⇌2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积减小的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动.
|
| A. | ①④ | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碘与氢气反应的热化学方程式
①I2(g)+H2(g) 2HI(g)△H=-9.48kJ/mol
2HI(g)△H=-9.48kJ/mol
②I2(s)+H2(g) 2HI(g)△H=+26.48kJ/mol
2HI(g)△H=+26.48kJ/mol
下列判断正确的是
A.254g I2(g)中通入2gH2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(ii)的反应物总能量比反应(i)的反应物总能量低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com