
【题目】右下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。

请回答下列问题:
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为: 。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置 (填“能”或“不能”)形成原电池,若不能,请说明理由;若能,请指出正、负极材料: 。当反应中收集到标准状况下224mL气体时,消耗的电极质量为 g。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的化学能直接转化为电能。
现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入 极(填a或b,下同),电子从 极流出,电解质溶液中OH-向 极移动。
(4)等质量的下列物质分别完全燃烧,放出热量较多的是 (填编号)
A.固体硫, B.硫蒸气.
科目:高中化学 来源: 题型:
【题目】由碳的氧化物直接合成乙醇燃料已进入大规模生产。
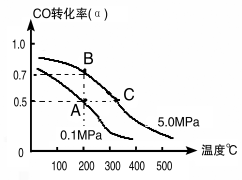
(1)如采取以CO和H2为原料合成乙醇,化学反应方程式:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) △H;若密闭容器中充有10 mol CO与20mol H2,在催化剂作用下反应生成乙醇,CO的转化率(α)与温度、压强的关系如下图所示。
CH3CH2OH(g)+H2O(g) △H;若密闭容器中充有10 mol CO与20mol H2,在催化剂作用下反应生成乙醇,CO的转化率(α)与温度、压强的关系如下图所示。
已知:2CO(g)+O2(g)===2CO2(g) △H1=-566kJ·mol-1
2H2(g)+O2(g)===2H2O(l) △H2=-572kJ·mol-1
CH3CH2OH(g)+3O2(g)===2CO2(g)+ 3H2O(g) △H3=-1366kJ·mol-1
H2O(g)===H2O(l) △H4=-44kJ·mol-1
①△H= kJ·mol-1
②若A、C两点都表示达到的平衡状态,则从反应开始到达平衡状态所需的时间tA tC(填“﹥”、“﹤”或“﹦”)。
③若A、B两点表示在某时刻达到的平衡状态,此时在A点时容器的体积为10L,则该温度下的平衡常数:K= ;
④熔融碳酸盐燃料电池(MCFS),是用煤气(CO+H2)作负极燃气,空气与CO2的混合气为正极助燃气,用一定比例Li2CO3和Na2CO3低熔点混合物做电解质,以金属镍(燃料极)为催化剂制成的。负极上CO反应的电极反应式为 。
(2)工业上还可以采取以CO2和H2为原料合成乙醇,并且更被化学工作者推崇,但是在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH 的平衡常数。请推测化学工作者认可由CO2制取CH3CH2OH的优点主要是: 。
(3)目前工业上也可以用CO2来生产甲醇。一定条件下发生反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。若将6mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如右图所示(实线)。
CH3OH(g)+H2O(g)。若将6mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如右图所示(实线)。

①请在答题卷图中绘出甲醇的物质的量随时间变化曲线。
②仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是 ,曲线Ⅱ对应的实验条件改变是 。
(4)将标准状况下4.48L CO2通入1L 0.3mol·L-1 NaOH溶液中完全反应,所得溶液中微粒浓度关系正确的是
A.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B.c(OH-)+c(CO32-)=c(H2CO3)+c(H+)
C.c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
D.2c(Na+)=3c(HCO3-)+3c(CO32-)+3c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”。工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2。
(1)亚氯酸钠也是一种性能优良的漂白剂,但在强酸性溶液中会发生歧化反应,产生ClO2气体,离子方程式为___________________________;向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为相同pH的硫酸,开始时反应缓慢,稍后一段时间产生气体速率迅速加快。产生气体速率迅速加快的原因是 。
(2)化学法可采用盐酸或双氧水还原氯酸钠制备ClO2。用H2O2作还原剂制备的ClO2更适合用于饮用水的消毒,其主要原因是 。
(3)电解法是目前研究最为热门的生产ClO2的方法之一。如图所示为直接电解氯酸钠、自动催化循环制备高纯ClO2的实验。
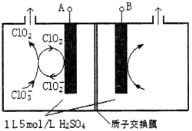
①电源负极为___________________极(填A或B)
②写出阴极室发生反应的电极反应式和离子方程式
_______________________ ___ ; 。
③控制电解液H+不低于5mol/L,可有效防止因H+浓度降低而导致的ClO2—歧化反应。若两极共收集到气体22.4L(体积已折算为标准状况,忽略电解液体积的变化和ClO2气体溶解的部分),此时阳极室与阴极室c(H+)之差为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料。某A1N样品仅含有A12O3杂质,为测定AlN的含量,设计如下三种实验方案。
已知:A1N+NaOH+H2O===NaA1O2+NH3↑
[方案Ⅰ]取一定最的样品,用以下装置测定样品中AlN的纯度(夹持仪器已略去)。

(1)上图C装置中球形干燥管的作用是________________________;
(2)完成以下实验步骤:组装好实验装置,首先________________再加入实验药品,接下来的实验操作是______________,打开分液漏斗活塞,加入浓溶液,至不再产生气体.打开K1,通入氨气一段时间,测定C装置反应前后的质量变化通入氮气的目的是________________________;
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见________________________;
【方案二】
用下图装置测定mg样品中A1N的纯度(部分夹持装置已略去);
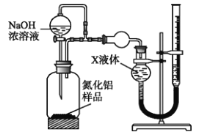
(4)为测定生成气体的体积,量气装置中的X液体可以是_________;
a.CCl4 b.H2O c.NH4Cl溶液 d.![]()
(5)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),则A1N的质量分数____________________;
【方案三】
按下图步骤测定样品中A1N的纯度:
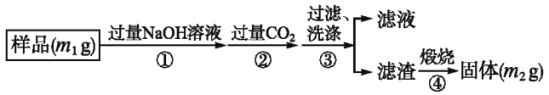
(6)步骤②生成沉淀的离子方程式为________________________;
(7)若在步骤③中未洗涤,测定结果将___________(填“偏高”“偏低’或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质谱图表明某有机物的相对分子质量为70,红外光谱表明有C==C和C==O的存在,1H核磁共振谱如下图(峰面积之比依次为1:1:1:3):分析核磁共振谱图,回答下列问题:
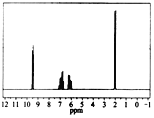
(1)分子中共有 种化学环境不同的氢原子。
(2)该物质的分子式为 。
(3)该有机物的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能的存储是其应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为________,该能层具有的原子轨道数为________。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2![]() 2NH3实现储氢和输氢。下列说法正确的是( )
2NH3实现储氢和输氢。下列说法正确的是( )
A.NH3分子中氮原子的轨道杂化方式为sp2杂化
B.NH4+与PH4+、CH4、BH4-、ClO4-互为等电子体
C.相同压强下,NH3沸点比PH3的沸点高
D.[Cu(NH3)4]2+中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空题
(1)已知断裂1 mol C-H, O=O,C=O,H-O化学键所需能量分别为a KJ,bKJ,cKJ,dKJ,则该反应CH4 + O2 = CO2 + 2H2O 的反应热为ΔH= kJ·mol-1
(2)N2H4是一种高效清洁的火箭燃料,0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则该反应的热化学方程式是 。
![]() (3)某元素的一种核素X的质量数为A,含有N个中子,则ag 1HmX分子中所含质子数是
(3)某元素的一种核素X的质量数为A,含有N个中子,则ag 1HmX分子中所含质子数是
(4)试比较下列三组ΔH的大小(填“>”、“<”或“=”)
A.A(g)+B(g) = C(g) ΔH1<0 A(g)+B(g) = C(l) ΔH2<0 则ΔH1____ΔH2
B.S(g)+O2(g) = SO2(g)ΔH1<0 S (s)+O2(g) = SO2(g) ΔH2<0 则ΔH1____ΔH2
C.C(s)+O2(g) = CO2(g)ΔH1<0 C(s)+O2(g) = CO(g) ΔH2<0 则ΔH1____ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一选修5:有机化学基础]
工业上可由A和环己烯(![]() )为原料合成某重要的有机物X、Y,路线如下(部分反应条件略):
)为原料合成某重要的有机物X、Y,路线如下(部分反应条件略):
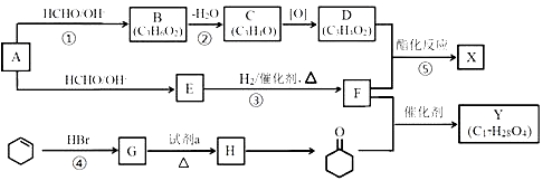
已知:Ⅰ.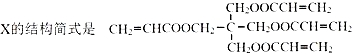
Ⅱ.![]()
Ⅲ.![]()
(1)B中含氧官能团的名称是___________。
(2)A的结构简式是______________。
(3)任选1种具有反式结构的C的同系物,用结构简式表示其反式结构_______。
(4)反应②、③、④、⑤中与反应①的类型相同的是_________。
(5)G→H的化学方程式是__________。
(6)E的结构构简式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如右图所示的原电池,下列说法正确的是( )。
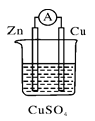
A.电流从锌电极通过电流表流向铜电极
B.锌电极发生还原反应,铜电极发生氧化反应
C.当有13 g Zn溶解时,外电路中就有0.4 mol电子通过
D.铜电极作正极,发生的电极反应为2H++2e-===H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com