

| A. | 铊元素的质量数是204.4 | B. | 铊原子的中子数为81 | ||
| C. | 铊对应的氢氧化物有两性 | D. | 铊元素位于第ⅢA族 |
分析 根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类,外围电子排布等,据此进行分析判断,
A.元素不谈质量数;
B.原子符号左上角的数字表示质子数;
C.同主族从上到下金属性增强,氢氧化物的碱性增强;
D.根据外围电子判断,Tl的外围电子排布为6s26p1.
解答 解:A.元素不谈质量数,TI元素的相对原子质量是204.4,故A错误;
B.原子符号左上角的数字表示质子数,铊原子的质子数为81,故B错误;
C.同主族从上到下金属性增强,氢氧化物的碱性增强,Tl与Al同主族,金属性大于Al,所以铊对应的氢氧化物的碱性大于氢氧化铝,显碱性,故C错误;
D.Tl的外围电子排布为6s26p1,为p区元素,处于第ⅢA族,故D正确;
故选D.
点评 本题考查对元素周期表的认识、核外电子排布规律、结构位置关系等,题目难度不大,注意对周期表的整体把握,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源: 题型:选择题
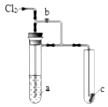 将氯气通入如图装置.若打开活塞,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,c很快褪色.则a溶液可能是( )
将氯气通入如图装置.若打开活塞,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,c很快褪色.则a溶液可能是( )| A. | 浓FeCl2溶液 | B. | 饱和KI溶液 | C. | 饱和食盐水 | D. | 浓NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都有气体产生 | B. | 最终产生的气体体积相同 | ||
| C. | ①中一开始就产生气体 | D. | ②中一开始不产生气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业合成氯化氢时使用过量氢气 | |
| B. | 硫酸工业接触室中使用过量空气 | |
| C. | 合成氨工业采用20~50 MPa高压 | |
| D. | 侯氏制碱法向母液中加入氯化钠提取氯化铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO+H2O→Ca(OH)2 | B. | 2Na+2H2O→2NaOH+H2↑ | ||
| C. | 2F2+2H2O→4HF+O2 | D. | 2H2+O2$\stackrel{点燃}{→}$2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W试剂 | 实验现象 | X、Y离子的推测 | |
| A | KI-淀粉溶液 | 溶液变蓝 | Fe3+、SO42- |
| B | 用pH试纸检测 | pH=7(常温) | CH3COO-、Na+ |
| C | 硝酸酸化的AgNO3溶液 | 白色沉淀 | CO32-、NH4+ |
| D | 过量NaOH溶液 | 无明显现象 | Al3+、Mg2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L CH4含有的共价键数为NA | |
| B. | 1 mol Fe与1mol Cl2充分反应,电子转移数为3NA | |
| C. | 常温下,pH=2的醋酸溶液中含有的H+数目为0.02NA | |
| D. | 常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com