
【题目】工业上用CO和H2反应制备二甲醚(CH3OCH3)的条件是压力2.0~10.0MPa,温度300℃。设备中进行下列反应,请回答下列问题:
①CO(g)+2H2(B)![]() CH3OH(g) △H=-90.7kJ/mol
CH3OH(g) △H=-90.7kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.2kJ/mol
CO2(g)+H2(g) △H=-41.2kJ/mol
(1)总反应3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g)的△H=_____________ 。据此可判断该反应_________________条件下自发。
(2)在温度和容积不变的条件下发生反应①,能说明该反应达到平衡状态的依据是_____
a.容器中压强保持不变 b.混合气体中c(CO)不变
c.v正(CO)= v逆(H2) d.c(CH3OH)= c(CO)
(3)在2L 的容器中加入amol CH3OH(g)发生反应②,达到平衡后若再加入amolCH3OH(g)重新达到平衡时,CH3OH 的转化率____________(填“增大”、“ 减小”或“不变”)。
(4)850℃时在一体积为10L 的容器中通入一定量的CO和H2O(g)发生反应③,CO和H2O(g)浓度变化如图所示。
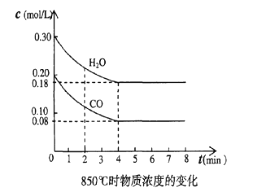
①0~4min 的平均反应速率,v(CO)=________________ 。
②若温度不变,向该容器中加入4mo1CO(g)、2mo1H2O(g)、3mo1CO2(g)和3molH2(g),起始时v正(CO)______v逆(H2)(填“<”、“ >”或“=”),请结合必要的计算说明理由。________。
【答案】 -246.1kJ/mol 低温 ab 不变 0.03mol/(L·min) < Qc = (0.3mol/L×0.3mol/L)/(0.4 mol/L×0.2 mol/L)=9/8,K = (0.12 mol/L×0.12 mol/L)/(0.08mol/L×0.18 mol/L)=1.0,因为Qc>K,平衡左移,所以v正<v逆。
【解析】(1)本题考查热化学反应方程式的计算,以及化学反应进行的方向,①×2+②+③得出:△H=[2×(-90.7)-23.5-41.2]kJ·mol-1=-246.1kJ·mol-1,根据△G=△H-T△S,△H<0,此反应△S<0,因此△G<0,条件是高温;(2)本题考查化学平衡状态的判断,a. 、根据化学反应方程式,反应前后气体系数之和不相等,因此当压强不再改变,说明反应达到平衡,故a正确;b、根据化学平衡状态的定义,因此混合气体c(CO)不变,说明反应达到平衡,故b正确;c、用不同物质的化学反应速率表示达到平衡,要求反应方向是一正一逆,且化学反应速率之比等于化学计量数之比,因此有2v正(CO)=v逆(H2),故c错误;d、因为没有说明开始时的投入量,因此c(CH3OH)= c(CO),不能说明反应达到平衡,故d错误;(3)本题考查化学平衡的移动,再加入amolCH3OH,相当于在原来的基础上增大压强,反应前后气体系数之和相等,因此增大压强平衡不移动,即CH3OH的转化率不变;(4)考查化学反应速率的计算以及Qc和K的关系,①根据化学反应速率的数学表达式,v(CO)=(0.20-0.08)/4mol/(L·min)=0.03 mol/(L·min);②Qc = (0.3mol/L×0.3mol/L)/(0.4 mol/L×0.2 mol/L)=9/8,K = (0.12 mol/L×0.12 mol/L)/(0.08mol/L×0.18 mol/L)=1.0,因为Qc>K,平衡左移,所以v正<v逆。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】在50mL18molL﹣1的浓H2SO4中加入足量的Cu片并加热,充分反应后,被还原的H2SO4的物质的量为( )
A. 等于0.9mol B. 等于0.45mol C. 大于0.45mol,小于0.9mol D. 小于0.45mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠的工艺流程如下:
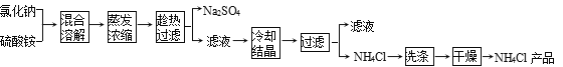
【查阅资料】
①上述流程所示物质中只有NH4Cl受热易分解:NH4Cl![]() NH3↑+HCl↑
NH3↑+HCl↑
②氯化铵和硫酸钠的溶解度随温度变化曲线如下图所示:
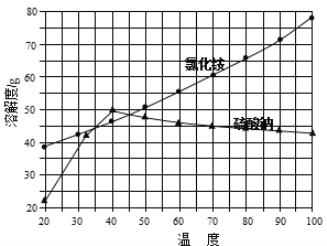
请回答下列问题:
(1)写出氯化钠和硫酸铵溶液混合得到硫酸钠晶体的化学方程式: 。
(2)欲制备10.7 g NH4Cl,理论上需NaCl质量为 g。
(3)实验室进行蒸发结晶用到的主要仪器除铁架台、铁圈、酒精灯外,还要有 。
(4)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为 。
(5)不用其它试剂,检查NH4Cl产品是否纯净的方法:
操作步骤 | 现象 | 结论 |
取少量氯化铵产品于试管底部, | 表明氯化铵产品纯净 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中。请回答下列问题:
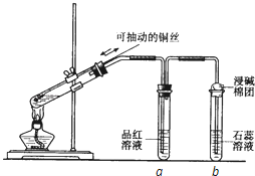
(1)写出铜与浓硫酸反应的化学方程式:________。
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用。
试管a中的现象是________, 作用是________;试管b中的现象是________,作用是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室提供如图1所示的仪器和高锰酸钾、石灰石、二氧化锰、稀硫酸、纯碱五种药品及火柴等相应物品:

(1)写出利用上述仪器和药品,用化学方程式表示制取该气体的化学反应原理________,在制取该气体的整个实验过程中需要用到的仪器有(填仪器序号)________;
(2)如果如图2所示用氯酸钾制氧气,请同学们将图补充完整;
(3)图中用此方法收集气体时.证明该气体己经收集满的现象是________;
(4)实验结束后要先________后________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化工专家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
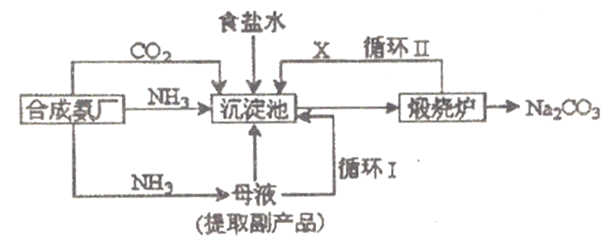
(1)上述流程中X物质的电子式为__________________。
(2)沉淀池中发生的化学反应方程式是_______________________,煅烧炉中发生的化学反应方程式是___________________________。
(3)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是______________________
(4)请你再写出一种实验室制取少量碳酸氢钠的方法:(用化学反应方程式来描述)_____________________________。
(5)某探究活动小组根据上述制碱原理,欲制备碳酸氢钠,同学按如下方案进行
实验:将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。

请回答:
①甲中发生反应的离子方程式是_____________________。
丁中发生反应的离子方程式是__________________。
②乙装置中的试剂是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下:
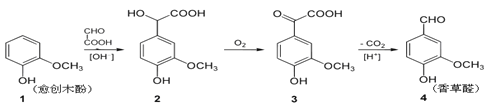
下列说法中正确的是
A. 反应1→2中原子利用率为90%
B. 检验制得的香草醛中是否混有化合物3,可用氯化铁溶液
C. 等物质的量的四种化合物分别与足量NaOH溶液反应,消耗NaOH物质的量之比为1∶4∶3∶2
D. 化合物2的分子式为C9H10O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验误差分析中,正确的是( )
A. 用湿润的pH试纸测稀碱液的pH值,测定值偏小
B. 用容量瓶配制溶液,定容时仰视刻度线,所配溶液浓度偏大
C. 用盐酸标准溶液滴定未知浓度的NaOH溶液时,若滴定前滴定管内无气泡,终点读数时有气泡,则所测NaOH溶液的浓度偏大
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com