


科目:高中化学 来源: 题型:
| A、将少量品红溶液分别滴入浓硝酸中和氯水中 |
| B、漂白粉及水玻璃长期暴露于空气中而变质 |
| C、酸性高锰酸钾溶液与亚硫酸钠溶液混合后褪色及硫酸铁溶液与淀粉碘化钾溶液混合后变蓝 |
| D、将适量Na2O2和Na分别加入硫酸亚铁溶液中;都能得到红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
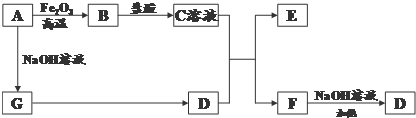
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
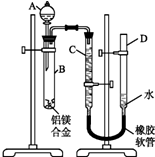 某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.
某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色透明的水溶液:K+、Na+、SO42-、MnO4- | ||
| B、0.1 mol?L-1 Na2CO3溶液:K+、Ba2+、NO3-、Cl- | ||
| C、PH=2的某溶液:K+、NH4+、Fe2+、NO3- | ||
D、
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com